서 론
급성 상부위장관 출혈의 원인은 다양하다(표 1). 소화성궤양이 약 절반을 차지하고 있어 가장 흔하고 식도 정맥류 출혈이나 식도-위 점막열상도 흔하다. 출혈성 소화성궤양은 내시경 기기와 방사선 중재술의 발전에도 불구하고 10~20%의 재출혈률과 5~10%의 사망률을 보이는 중요한 질환이다. 사망률이 현저히 감소하지 않는 이유는 (1) 환자의 고령화 (2) 고혈압, 당뇨, 심혈관계 질환, 악성질환 등을 가진 환자 증가(3) 아스피린이나 클로피도그렐과 같은 항혈소판제, 비스테로이드소염제, 스테로이드 등을 복용하는 환자 증가 (4) 헬리코박터필로리(Helicobacter pylori) 음성 소화성궤양 증가 등으로 추정된다. 최근 국내에서 소화성궤양의 예방과 치료에 관한 가이드라인 6개가 발표된 바 있는데1-6) 본고에서는 이들을 중심으로 출혈성 소화성궤양의 치료에 대하여 살펴보기로 한다.
상부위장관 출혈 환자의 응급처치
상부위장관 출혈 환자의 치료에서 우선 고려할 점은 혈관 내 혈액량과 혈동학적인 안정성을 적절하게 유지하는 것이다. 응급실에 환자가 내원하면 즉시 생체징후를 확인하고 18게이지 이상의 정맥주사경로를 확보할 필요가 있다. 혈압이 낮으면 쇼크 자세를 유지하고, 토혈의 경우에는 기도 흡인을 방지하기 위하여 왼쪽 측와위 자세를 유지한다. 출혈의 원인을 확인하기 위해 기저질환 유무, 항혈소판제나 비스테로이드소염제 등 약제 복용 유무, 음주력, 궤양 출혈의 과거력 등을 확인하다. 수혈은 혈색소 10 g/dL을 목표로 한다7). 그러나 다량의 급성출혈에서는 혈액검사 결과와 무관하게 수혈을 준비하는 것이 좋다.
비위관(nasogastric tube)을 이용한 위세척이 꼭 필요한지는 불명확하다. 한 연구에서 비위관 흡입법의 상부위장관 출혈 확인 민감도는 42%에 불과하였다8). 활동성 출혈이 멎었거나 큰 혈괴가 형성된 경우, 십이지장 출혈 등에서 비위관으로 혈액이 나오지 않을 수 있기 때문이다. 과거에는 차가운 식염수로 반복 세척하여 지혈효과를 기대하였지만 이러한 관행의 치료효과는 더 이상 인정되지 않고 있다. 대량 출혈 시 내시경 시야 확보를 위하여 비위관세척을 시도할 수 있으나 단단하고 큰 혈괴는 제거되지 않는다. 혈액과 혈괴는 위저부에 모이기 때문에 비위관 세척을 하지 않아도 전정부, 위각부, 위체부소만 및 들문(cardia) 병소는 대부분 관찰하고 치료할 수 있다. 요컨대, 비위관 세척의 유용성은 생각보다 크지 않으며, 비위관 세척을 위하여 내시경 검사를 연기해서는 안 된다.
내시경 검사
소화성궤양 출혈이 의심된 환자에서 일찍 내시경 검사를 시행하는 것은 중요하다. 정확한 진단을 내릴 수 있을 뿐만 아니라 내시경 치료도 가능하기 때문에 수시간 이내에 시행해야 한다9). 특히 기립성 저혈압이나 쇼크가 발생하였던 경우, 다량의 수혈이 필요한 경우, 혈색소가 10 g/dL 이하로 감소한 경우, 정맥류 출혈이나 재발 출혈이 의심된 경우, 수술이나 혈관조영술을 고려하는 경우에는 신속히 내시경 검사를 시행한다. 그러나 급성 심근경색증, 심한 만성 폐쇄성 폐질환(산소 포화도 90% 이하), 혈동학적으로 불안정한 경우, 환자가 매우 불안해 하는 경우 등은 상대적 금기증이므로 치료내시경이 필요한 경우에 국한하여 시행한다.
출혈성 궤양의 내시경 소견은 Forrest 분류에 따라 기술한다(표 2)10). 이 분류법은 재출혈 가능성을 예측하는 데 유용하다. 활동성 출혈인 Ia와 Ib에서는 당연히 내시경 지혈술이 필요하다. 노출혈관을 의미하는 IIa의 경우도 거의 50%의 환자에서 재출혈을 보이기 때문에 예방적 내시경 지혈술이 필요하다. IIb에서 예방적 내시경 지혈술의 필요성은 불명확하다. IIb 병소에서 혈괴를 제거한 후 종종 노출혈관이 발견되므로 치료가 필요하다는 의견과 혈괴제거 도중 출혈이 발생할 위험이 있다는 우려가 있다. 환자의 상태와 병소의 위치 및 각 의료기관의 상황에 따라 적절히 선택해야 한다. 재출혈 저위험군으로 분류되는 IIc와 III에서는 내시경 지혈술이 필요 없다.
고위험군으로 분류된 환자는 입원치료를 요한다. 환자의 상태에 따라서 첫 24시간 혹은 48시간 동안 집중 치료실 입원이 필요할 수 있다. 60세 미만, 혈압과 맥박이 안정적이고, 수혈 없이 혈색소가 8~10 g/dL로 유지되고, 심한 동반 질환이나 응고 장애가 없고, 병원 밖에서 출혈이 발생하였고, 내시경에서 Forrest 분류 IIc 혹은 III이고, 재출혈시 즉시 병원을 방문할 수 있고, 적절한 가족의 지지가 있는 경우에는 외래기반으로 치료하기도 한다.
내시경 치료
내시경 치료는 소화성궤양 출혈 환자의 재출혈률, 수술률 및 사망률을 감소시킨다4). 내시경 지혈술은 접촉법과 비접촉법으로 나뉜다. 접촉법에는 국소주입법, 전기응고소작법, 열탐침법(heat probe), 헤모클립을 이용한 기계적 지혈술 등이 있다. 비접촉법에는 아르곤 플라즈마 응고법(argon plasma coagulation)과 레이저 소작법(laser ablation)이 있다. 급성 소화성궤양 출혈의 80~90%에서 내시경으로 지혈이 가능하다. 비접촉법에 비하여 접촉법의 지혈률이 좋다. 접촉법에서 서로 다른 방법 간 지혈률 차이는 없다. 두 가지 이상의 치료법을 함께 시행하는 내시경 병합 치료가 권장되고 있지만 기계적 지혈술 혹은 전기응고소작법 단독에 비해 더 효과적인지 확실치 않다4). 결국 여러 내시경 치료 방법의 결과는 크게 다르지 않기 때문에 각 내시경실에서 신속히 준비할 수 있고, 내시경의가 가장 익숙한 지혈 방법을 선택하는 것이 좋다9,11).
출혈성 소화성궤양 내시경 치료의 실패 요인은 (1) 소화성궤양의 과거력 (2) 궤양 출혈의 과거력 (3) 내원 시 쇼크 (4) 활동성 출혈 (5) 직경 2 cm 이상의 큰 궤양 (6) 2 mm 이상의 큰 혈관 (7) 위 소만, 십이지장 구부 상부 또는 후부에 위치한 궤양 등이다12,13). 내시경 지혈술 24시간 이내에 시행하는 2차 내시경(second-look endoscopy)은 과거에 널리 시행되었지만 최근에는 권장되지 않고 있다. 비록 메타 연구에서 다소 유용하다고 분석된 바 있지만, 그 효과가 약간의 재출혈 감소에 불과하였다14). 따라서 2차 내시경은 임상적으로 재출혈 징후가 있거나 초기 치료의 지혈 효과가 불확실한 경우에 한하여 고려하는 것이 좋다. 위궤양은 함몰형 조기위암과 구분이 쉽지 않다. 첫 내시경 검사에서 조직검사가 시행되지 않았고 위암이 의심되는 경우에는 가급적 빨리 내시경 재검을 하는 것이 좋다.
산분비 억제 치료
위산은 혈액 응고 과정을 어렵게 하고 응집된 혈소판과 섬유소를 용해시킨다. 위산 분비를 억제하여 위내 산도를 pH 6 이상으로 유지시키면 혈액 응고 과정이 안정화되어 재출혈이 감소한다. H2 수용체 길항제는 위산분비 억제력이 약하고 약제내성의 문제가 있다15). 프로톤펌프억제제(proton pump inhibitor, PPI)는 위산분비 억제력이 강하고 약제내성이 발생하지 않아 H2 수용체 길항제보다 유리하다. 메타 연구에서 프로톤펌프억제제는 출혈성 소화성궤양의 재출혈률과 수술률을 낮추는 것으로 분석되었다16). 과거 omeprazole 80 mg을 신속히(bolus 혹은 loading으로) 정주한 후 72시간 동안 8 mg/hour로 연속 주입하는 방법이 소개되었다. 최근에는 pantoprazole과 esomeprazole 정주형 제형이 사용 가능해졌다. 과거에는 내시경 지혈술을 시행한 후 프로톤펌프억제제를 시작하였다. 그러나 투약시점을 내시경 지혈술 이전으로 앞당기는 것이 유리하다는 연구결과가 발표된 후17) 최근에는 고용량 프로톤펌프억제제를 일찍 투여한다.
수술 치료 및 방사선 중재 치료
내시경 치료와 산분비 억제 치료의 발달에도 불구하고 상부위장관 출혈에서 수술 치료는 여전히 중요하다4). 출혈성 소화성궤양의 초치료는 내시경 지혈술이다. 하지만 소화성궤양 출혈을 항상 내시경으로 지혈시켜야 한다는 선입견 때문에 수술의뢰 시점이 늦어져 환자를 위험에 노출시키는 것은 좋지 않다. 수술 치료를 의뢰하는 적응증은 (1) 치명적 대량 출혈 (2) 하루 5단위 이상 수혈을 요하는 지속적 출혈 (3) 출혈이 2~3회 이상 반복될 때 (4) 궤양 기저부에 노출혈관이 보이고 내시경 치료에도 불구하고 지혈되지 않을 때 등이다.
혈관 조영술과 색전술(emblolization)은 내시경으로 출혈 부위를 찾지 못했거나 내시경 지혈술이 실패하였을 때 사용하는 비수술적 방법이다4,18). 색전술의 초기 지혈 성공률은 52~94%이며, 색전술이 필요한 정도의 재출혈률은 약 10%이다. 드물지만 장허혈, 십이지장 폐쇄 및 위, 간, 비장 경색 등의 합병증이 가능하다. 방사선 중재 치료는 내시경 치료에 실패한, 특히 수술 고위험군 환자의 치료에 주로 이용되고 있다. 출혈 후 가급적 이른 시간에 색전술을 시행해야 지혈 성공률이 높다. 다른 모든 방법을 다 써 본 후 마지막 수단(last resort)으로 색전술을 선택하는 것은 좋지 않다18).
헬리코박터 감염의 치료
출혈성 소화성궤양의 재발방지를 위하여 헬리코박터 감염을 진단하고 치료하는 것은 매우 중요하다19). 다만 출혈 시점의 헬리코박터 검사는 진단의 양성률이 낮다는 점, 즉 위음성이 가능하다는 점을 고려해야야 한다. 첫 검사에서 헬리코박터 음성인 환자에서는 추후 재검하는 것이 좋다. 헬리코박터 제균치료 시점에 대한 의견은 다양하다. 대한소화기학회의 설문조사에 따르면 퇴원 후 첫 외래 방문 시 제균 요법을 처방하는 것이 선호되고 있다4). 최근 헬리코박터 감염에 대한 표준적 초치료의 제균 성공률이 80%를 밑도는 상황이므로 이에 대한 대책이 필요하다1).
비스테로이드소염제와 저용량 아스피린 사용자
비스테로이드소염제나 항혈소판제를 사용하는 환자에서 출혈성 궤양이 발생한 경우 가급적 약제를 중지하는 것이 좋다. 비스테로이드소염제를 끊을 수 있는 환자의 소화성궤양 치료는 비스테로이드소염제를 사용하지 않는 환자에서 발생한 소화성궤양의 치료와 동일하다5). 비스테로이드소염제를 계속 복용해야 할 경우 궤양 치유를 촉진하기 위하여 프로톤펌프억제제를 사용한다. 정해진 치료기간은 없지만 궤양이 크거나 비스테로이드소염제를 계속 사용하는 경우 장기간 프로톤펌프억제제 투약이 필요하다. 소화성궤양 치료 종료 후 비스테로이드소염제를 계속 사용해야 할 경우에는 소화성궤양 예방을 위한 조치(COX-2 억제제의 사용, 프로톤펌프억제제 혹은 미소프로스톨의 병용투여)가 필요하다5). 저용량 아스피린을 사용하는 환자에서 발생한 소화성궤양의 치료와 예방법은 일반적인 비스테로이드소염제 관련 소화성궤양과 동일하다.
퇴원 후 외래에서의 환자 관리
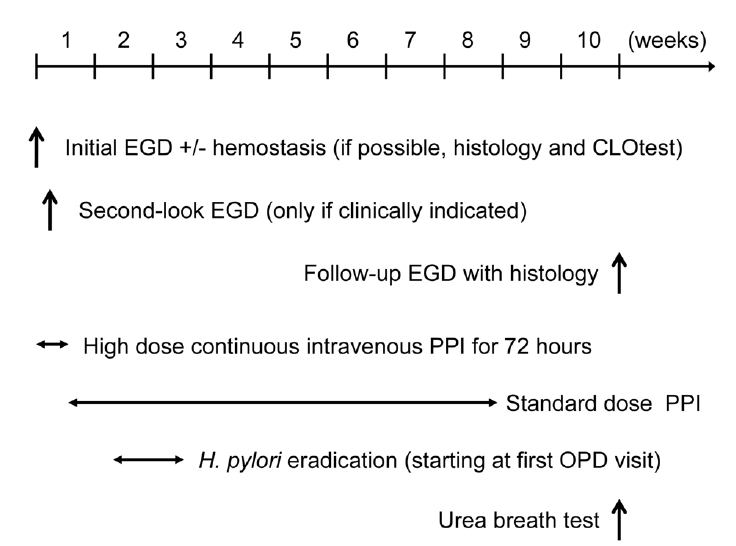
퇴원 후 4~8주까지 위산분비 억제제를 투여하면서 흡연, 진통소염제, 음주, 자극적인 음식, 스트레스 등 위험인자를 피하도록 권하는 것이 좋다. 투약 종료 시점에 내시경 재검을 시행하여 출혈병소가 완전히 호전되었는지 확인해야 한다. 십이지장궤양 출혈에서 내시경 재검이 필요한가에 대하여 논란이 있지만 필자는 재검을 권하는 편이다. 위궤양 출혈에서는 반드시 내시경 재검이 필요하다. 위궤양 출혈의 첫 내시경 검사에서 조직 검사가 빠지는 경우가 많고, 함몰형 조기 위암은 양성 위궤양과 감별이 어렵기 때문이다. 첫 내시경에서 양성 위궤양으로 진단된 경우라 하더라도, 약물치료 후 내시경 재검을 통하여 악성궤양이 아님을 확실히 감별해야 한다. 적절한 치료와 위험인자에 대한 관리에도 불구하고 궤양재발이 반복되는 환자에서는 수년 이상 장기간 위산분비 억제치료를 권할 수 있다. 그림 1에 필자가 위궤양 출혈을 치료하는 표준 방법을 정리하였다.
결 론
내시경 기술과 약물치료의 발달에도 불구하고 출혈성 소화성궤양의 높은 사망률과 재출혈은 중요한 문제가 아닐 수 없다. 필자는 출혈성 소화성궤양 환자의 관리에서 다음 몇 가지를 강조하고 싶다. (1) 고용량 프로톤펌프억제제를 일찍 투여하여 재출혈률과 수술률을 낮추자. (2) 내시경 지혈술을 익히되 내시경 이외의 방법이 있음을 잊지 말자. (3) 내시경 재검을 통하여 악성질환이 아님을 확실히 감별하자. (4) 항혈소판제나 비스테로이드소염제를 복용하고 있는지 꼼꼼히 확인하고 필요하면 예방대책을 강구하자. (5) 헬리코박터 감염자에서 제균치료를 시행하고 반드시 제균성공 여부를 확인하자.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print