만성췌장염의 병리는 췌장 섬세포와 췌관세포의 계속적이고 비가역적인 파괴를 특징으로 하며 이 세포들은 섬유조직과 세포 외 기질로 대체된다. 심한 췌장염은 그 후유증으로 조절되지 않는 통증, 당뇨, 그리고 췌장부전을 남긴다[3]. 만성췌장염의 병리기전은 만성 알코올 중독에 의한 췌장염을 제외하고는 아직 확실히 밝혀지지 않았다. 알코올에 의해 만성 췌장염이 생기는 기전은 과량의 알코올의 지속적인 섭취로 췌장액내의 지질분해효소, 키모트립신, 그리고 중탄산염의 양이 감소하고 췌장액 자체의 양도 감소한다[4]. 혈액내의 단백질농도가 상승하게 되고 췌장액의 점도가 증가하여 단백전색(protein plug)이 발생하고 이 단백전색에 의해 췌관이 폐쇄되고 췌관의 확장 및 협착 등의 이상이 초래된다. 이 단백전색에 칼슘이 침착되어 췌실질의 석회화와 췌석 등이 발생하게 되며 췌석에 의한 췌관의 폐쇄도 췌실질의 염증을 일으켜 동일한 과정을 밟는 악순환으로 들어선다[5,6]. Sakakibara 등은 실험동물에서 췌관의 부분폐쇄를 시킨 후 1년경과 후에 약 64%에서 췌석이 나타난 것을 보고하였고 단백질이 풍부한 췌장 분비액의 저류가 결석을 형성한다고 하였다[7].
만성췌장염의 주 증상으로는 상복부 동통이 반복적으로 나타남을 호소하는 경우가 가장 흔하며, 병이 진행되면 췌장의 외분비기능장애에 따른 지방성 대변과 체중감소 등이 나타나며 내분비기능장애로 인한 당뇨가 발생한다. 통증 없이 지방변, 체중 감소, 당뇨 등의 증상을 보이는 경우도 드물게 있지만 통증은 거의 모든 환자에서 나타나며 발작적이고 지속적인 것이 특징이며 심한 통증으로 마약중독이 되는 경우도 있다[6].
췌장염에 의해 통증이 생기는 기전은 복합적인 원인에 의한 것으로 보이며 두 개의 보완적인 가설이 외과적인 치료의 근간이 된다. 첫 번째는 췌장구획설(pancreatic compartment theory)로 만성췌장염 시 췌관내압(20-80 mmHg)과 간질내압(50-250 mmHg)이 정상(7-15 mmHg, 20 mmHg)에 비하여 증가되어 국소적인 내장구획증후군(visceral compartment syndrome)을 일으키고 이것이 통증을 유발한다는 것이다. 두 번째는 췌장주위신경의 염증에 의한 것으로 췌장간질과 췌장주위의 신경에 파급된 염증으로 인해 분비된 여러 가지 시토카인(cytokine)들이 통각수용기를 자극하여 통증이 생긴다는 설로 이 두 개의 이론이 복합적으로 작용하여 통증을 일으키는 것으로 생각된다. 이러한 이론은 만성췌장염 시 수술적 치료 즉 절제가 통증을 없애는 데 타당하다는 사실을 시사해 준다[8].
만성췌장염의 합병증으로 인한 증상은 황달과 위장관 출혈 등이 있다. 황달은 췌두부의 섬유화로 인하여 충수담관의 협착이 유발되어 발생한다. 위장관 출혈은 비교적 드물지만 비장정맥 혈전에 의하여 좌측 문맥압 항진증이 유발되고 이에 따른 위정맥류로 발생하게 된다. 또한 가성 낭종이 동반되기도 한다.
수술적 치료의 적응증은 반복적이고 참기 어려운 통증에 의한 경우가 가장 많고, 췌장의 내분비 외분비 기능의 더 이상의 파괴를 막기 위하여, 가성 낭종이나 담관 십이지장의 폐쇄, 췌장농양 누공의 형성, 우측문맥 고혈압 등의 합병증에 의한 경우, 그리고 췌장암과의 구별이 불가능한 경우 등을 들 수 있다. 수술은 적어도 식사 후의 동통, 위하부 소화관의 폐쇄, 담도의 폐쇄, 또는 내 소장루 등으로 인하여 영양적, 대사적 장애가 일어나기 전에 고려되어야 하며, 특히 환자가 통증에 의하여 진통제에 비가역적인 중독이 되기 전에 이에 대한 수술이 고려되어야 한다().
Surgical indication of chronic pancreatitis
또한 췌관의 결석은 반드시 췌관의 협착과 연관이 있다. 췌관 결석은 내시경적인 치료와 수술적 치료로 접근할 수 있다. 내시경적 치료는 협착의 확장과 결석의 제거 그리고 스텐트의 삽입으로 이루어진다. 유럽에서는 체외 충격파 쇄석술도 사용되고 있다. 수술적 치료로는 주췌관내 결석이 있을 경우는 결석을 제거하고 감압술을 시행하지만 췌두부와 갈고리돌기에 있을 경우 절제술이 적응증이 된다[3]. 췌결석이 두부의 주체관에 있을 경우 췌십이지장절제술은 안전하고 필요충분조건을 만족하는 치료라고 할 수 있다. 특히 만성췌장염 중 췌석이 동반된 경우는 내시경적 제거가 어렵고 재발가능성이 많으며 담도의 협착이 잇는 경우가 많아 수술적 치료가 더욱 필요하리라 사료된다. 더구나 결석을 동반할 때는 단순 만성췌장염에 비하여 췌장암이 발생될 가능성이 4배에 달하므로 수술적인 절제술이 더욱 타당하다고 할 수 있다.
만성췌장염의 수술 시기는 문헌마다 차이는 있지만 우선 내과적인 치료를 시행하다가 치료에 반응이 없을 때 시행하는 것이 전반적인 치료방침인데 환자들의 자연경과를 보면 3-4년 후에 내과적 치료를 한 후에 50-80% 정도의 통증의 소실을 경험하는 것으로 보고가 되고 있다. 하지만 내과적 치료가 주로 통증완화에 국한이 되어 있기 때문에 통증이 없더라고 췌장 내분비 및 외분비기능은 지속적으로 감소할 수 있기 때문에 적극적으로 수술을 권장하는 보고도 있다[9]. 일반적으로 내과적 치료를 3년 정도 시행 후 치료가 어려운 경우 수술을 시행하는 것이 좋다는 보고도 있다[10].
만성췌장염의 수술적 술기는 직접적인 방법과 간접적인 방법으로 두 가지로 크게 나눌 수 있고 간접적인 방법은 위장 또는 담도의 배액술, 췌관괄약근 절제술이나 괄약근 성형술, 췌장주위의 신경 절제술 등이 있다. 직접적인 술기로는 췌장관의 내 배액술, 절제술, 절제술과 췌장 도세포의 자기 이식, 그리고 췌장관의 결찰 등이 있다. 또 다른 분류 방법으로 나누면 췌관배액술, 췌절제술, 혹은 신경절제술의 세 가지로 나눌 수도 있다[10].
담도배액술은 급성 담도염, 담도 결석형성, 이차적인 폐쇄성 간경화, 그리고 한 달 이상 지속되는 황달 등이 적응증이 된다. 또한 영상검사상 담도의 폐쇄가 있거나 담도염의 과거력이 있는 환자에서도 고려할 수 있다[11,12].
담도배액술의 하나인 괄약근 성형술은 췌장관 전체가 일정하게 늘어나 있으면서 주 췌장관의 개구부에 폐쇄가 있는 경우에 적응증이 되지만[11,12] 만성췌장염에서 이러한 환자는 흔하지 않고 현재는 내시경을 사용하여 괄약근 성형술을 시행하는 경우가 많다[13-18]. 1911년 Link [19]에 의하여 체외배액술이 시행된 이후에 1954년 DuVal [20]은 췌장 미부를 절제하고 공장을 이용하여 공장과 췌장을 단단 문합하여 췌관을 배액한 수술을 시행하였으나 수술결과가 양호하지 않아서 현재는 많이 사용되고 있지는 않다(). 1958년 Peustow와 Gillesby [21]는 측측 췌공장문합술을 시행하여 수술 후 통증 소실의 효과도 좋았고 특히 여러 곳에 췌관의 협착이 있는 경우에 증상 호전이 확실히 있었으나 췌미부를 절제하면서 비장절제를 같이 시행하여야 하는 단점이 있었다(). 1960년 Partington과 Rochelle [22]에 췌장 미부나 비장을 절제하지 않아서 췌장 절제로 인한 당뇨의 악화를 줄일 수 있고 췌장주위의 혈관에 생길 수 있는 합병증을 줄일 수 있게 췌관을 췌미부부터 췌두부까지 종으로 절개하여 췌관과 공장을 측측 문합을 하는 술기로 변형되었으며 현재 가장 흔하게 사용되는 술기가 되었다(-). 이러한 췌관 배액술을 췌관의 확장이 동반된 경우 즉 췌관이 최소한 7-8mm 이상은 되어야 시행되며, 80% 이상의 환자에서 통증의 소실을 보고하고 있다. 저자들의 경우에 있어서도 췌관의 확장이 동반된 13예에서 측측췌공장문합술 11예, 그 외 췌미부 절제 및 단단췌공장문합술을 2예에서 시행하였으며 그중 91%에서 통증의 소실이나 감소율을 경험하였다.
Peustow and Gillesby procedure.
Partington and Rochelle procedure.
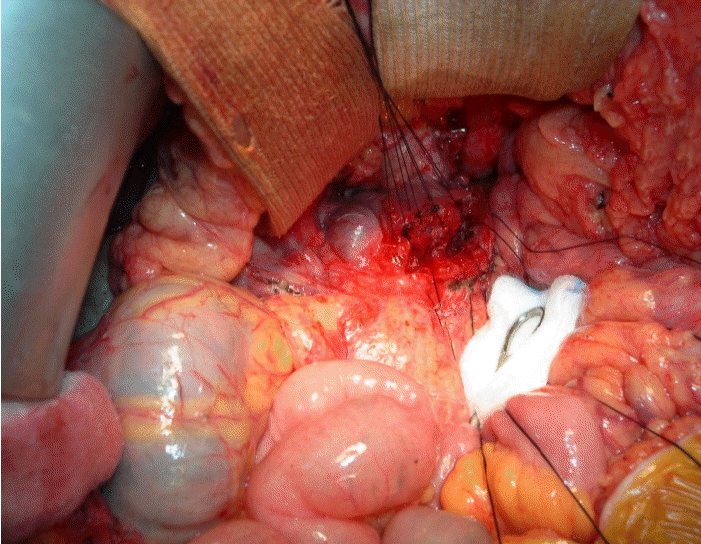
Partington and Rochelle procedure. Operative finding of chronic pancreatitis patients. Dilated pancreatic duct was open and pancreatic stones were removed prior to side to side pancreaticojejunostomy.
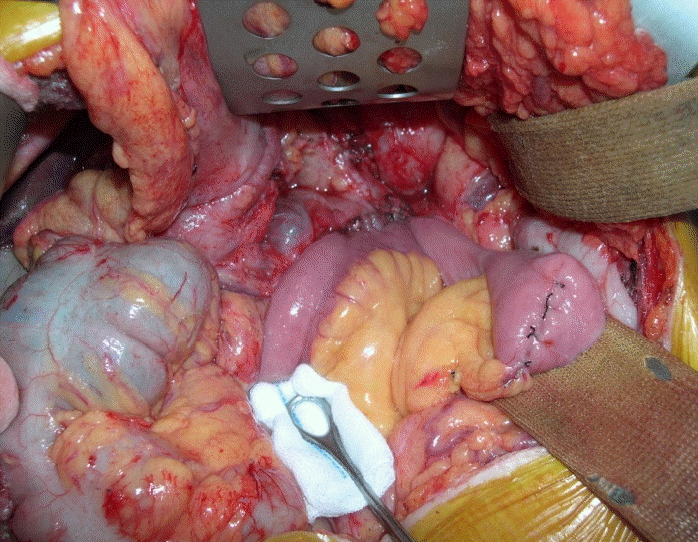
Partington & Rochelle procedure. Operative finding of chronic pancreatitis patients. Dilated pancreatic duct was ypassed with side to side pancreaticojejunostomy.
췌장절제는 배액술이 불가능하거나 적당치 않은 경우, 췌실질의 대부분이 소실된 말기의 경우, 술 전 이미 내분비 외분비 기능의 심한 저하가 있는 경우, 기존의 배액술로 통증이나 다른 증상의 호전이 없는 경우 등에서 시행하게 된다. 췌장의 절제술식은 1944년 Priestley 등[23]에 의하여 췌전절제술이 시행되었고 1946년 Whipple [24]에 의하여 췌십이지장절제술이 시행되었다. 1958년 Eliason과 Welty [25]에 의하여 미부 췌장절제술이 처음 시도되었고, 1978년 Traverso와 Longmire [26]에 의하여 유문부 보존 췌십이지장 절제술이 시행되었다(). 췌장절제술은 주 병변의 위치에 따라 다양하게 시술된다. Moosa [27]는 만성췌장염 시 췌십이지장절제술이 추천되는 이유를 다음과 같이 정리하였다. 첫째, 만성췌장염시 세포의 변화는 주로 췌두부와 갈고리돌기(uncinate process)에서 일어난다. 둘째, 췌장섬세포의 대부분은 췌체부와 체미부에 존재한다. 셋째, 담도와 십이지장의 폐쇄가 해결된다. 넷째, 현미경적인 수준의 놓칠 수 있는 췌장암이 수술로 완치된다[27-33].
Pylorus preserving panceaticoduodenectomy.
췌전절제술은 병변이 전 췌장을 모두 포함하거나 췌장의 부분절제술로 통증이 완화되지 않거나 재발한 경우, 그리고 이미 췌장의 내분비, 외분비기능이 거의 소실된 경우에 적응증이 된다. 췌전절제술을 시행한 후에는 췌장효소와 인슐린의 공급이 필요하며 혈당의 조절이 쉽지 않아 세심한 관찰이 필요하다[34-36]. 미부 췌장절제술은 만성 췌장염으로 수술한 환자의 5-15% 정도를 차지하며 질환이 췌장의 미부와 체부에 국한된 질환과 췌장관의 지름이 5 mm 이하인 경우 시행하게 되며 Sawyer와 Frey [37]는 90%에서 평균 4년 이상의 통증완화의 결과를 보고하였다. 저자들의 경우에 있어서도 췌관의 확장이 동반된 31예에서 췌십이장절제술 14예, 그 외 췌미부절제 17예에서 시행하였으며 그중 87%에서 통증의 소실이나 감소를 경험하였다.
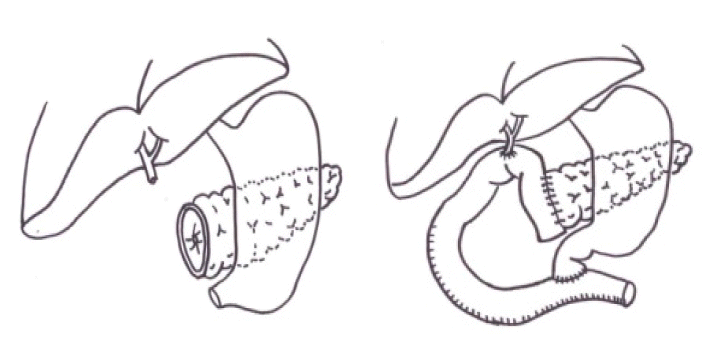
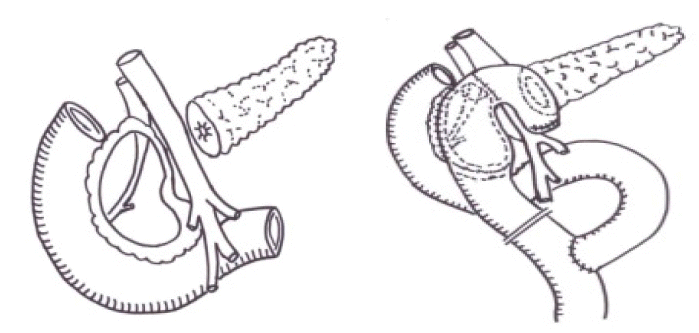
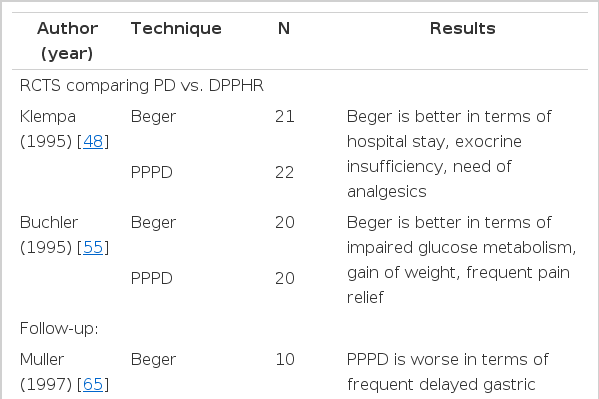
병변이 주로 두부에 존재하며 배액술을 시행할 정도의 췌관확장이 없는 경우 그리고 십이지장이나 담도의 폐쇄가 동반된 경우 췌두부절제술을 시행한다[38-41]. 십이지장이나 담도의 폐쇄가 없는 경우는 십이지장을 보존하는 췌두부절제술을 시행하기도 한다. 이러한 수술을 시행하게 되면 십이지장을 보존하게 되므로 각종 위장관 호르몬의 분비가 정상적으로 유지가 되며 조절이 가능하며 추가로 췌두부를 절제함으로써 만성췌장염의 진행을 정지시킬 수 있고 술식에 따라서는 가능하면 총수담관의 폐쇄도 한번에 해소할 수 있는 술식이다[38-41]. 수술사망률이 다른 수술들에 비해서 적고 당뇨발생률이 5-10% 내외이고 통증 소실률이 80% 이상 되기 때문에 결과가 비교적 양호한 수술법이다. 이러한 십이지장 보존 췌장두부절제술은 미부췌장과 공장을 단단문합하는Beger 술식[42-44], 측측문합하는 Frey 술식[45,46], Beger 술식에서 췌장미부공장문합을 생략하게 한 Bern 술식[47] 등으로 나눈다.
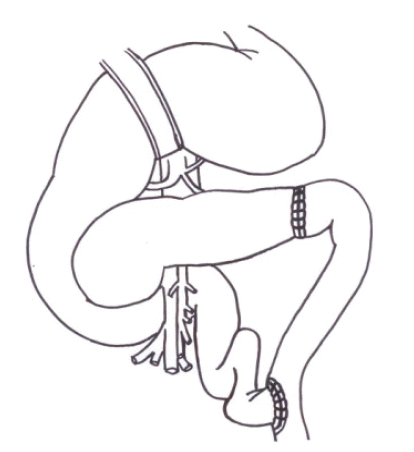
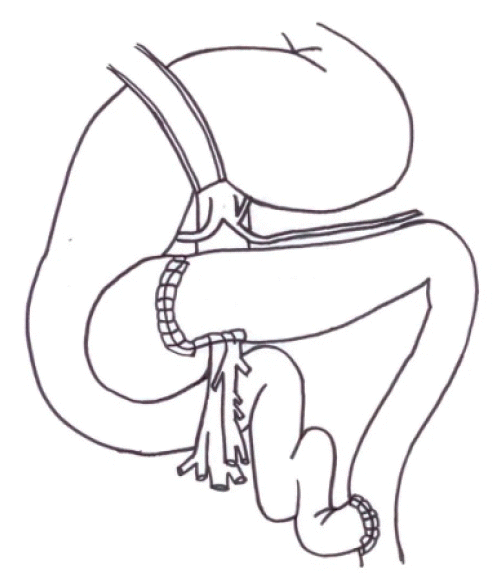
Beger 술식[42-44]은 췌장 미부나 췌부의 췌관이 확장되있지 않았을 때 시행하게 되는데 췌장을 문맥 위에서 분리하여 췌두부를 절제해내고 공장으로 췌미부의 췌관은 단단 문합하고 췌두부의 췌관은 측측 문합하는 방법으로 췌관의 배액술을 시행한다(). Frey 술식[45,46]은 췌두부의 복측벽을 절제해내서 췌두부의 췌관을 완전히 감압하고 췌석도 제거를 한 후에 공장을 이용하여 췌두부에서부터 췌미부까지 측측문합을 하는 것으로서 Beger 술식과 다른 점은 췌장을 분할하지 않는 것이다(). 이에 반해 Bern 술식[47]은 Beger 술식과 췌두부의 수술은 동일하나 췌장을 절단하지 않는 것이 달라서 문합은 췌장 두부와 공장을 한 번만 측측 문합하면 된다().
만성 췌장염에 대한 수술로 여러 가지 수술법들이 개발이되었고 비교가 되었지만 지금까지의 결과는 다른 모든 수술보다 월등히 좋은 수술보다는 그 환자에 맞는 환자에 증상과 상태에 따른 적절한 치료법을 선택하는 것이 좋을 것으로 사료된다(). 또한 이러한 모든 수술을 동시에 비교하는 것이 현실적으로 어렵기 때문에 앞으로의 무작위적인 잘 짜인 연구가 필요할 것이 절실하다[48-65].
Comparison of surgical outcome of chronic pancreatitis
또한 만성 췌장염에 의한 통증과 합병증의 치료는 수술로 기대할 만한 결과를 얻을 수 있지만 계속적으로 진행하는 내분비, 외분비기능의 저하에 대한 해결방법을 제시해 주지는 못한다. 만성 췌장염에 의한 당뇨의 해결을 위하여는 자가췌장 또는 기증췌장의 도세포이 식과 췌장이식 등이 있다. 1977년 Najarian 등[66]에 의하여 사람에 있어서 첫 번째 췌장 자가 도세포이식이 시행되었다. 도세포이식은 술기가 비교적 간단한 반면에 도세포 분리에 따른 수적 확보의 어려움, 간 내 주입 후 착상의 어려움 그리고 이식 후 야기되는 거부반응의 진단과 치료의 어려움 등이 아직 해결되지 못하고 있다. 한편 췌장이식은 수술 후 면역반응과 그에 대체로 면역억제제를 사용해야 하나 현재 도세포이식에 비해 더 효과적인 당뇨의 조절을 기대할 수 있는 것으로 보고되고 있다[67-72].
신경절제술은 이론적으로는 췌실질에 손상을 주지 않아 이상적인 방법이다. 내장신경절제술과 복강신경절제술이 처음에는 좋은 결과를 보여서 많이 시행이 되었으나 추적조사에서 인정을 받지 못해서 현재는 많이 사용되고 있지 않은 술식이다. 최근에 흉강경을 이용한 방법들이 개발이 되고 시행되고 있지만 지속적인 추적관찰이 필요하다고 하겠다[73-81].
References
1. Kim CD. Current status of acute pancreatitis in Korea. Korean J Gastroenterol 2003;42:1–11.
2. Kang MS, Lee YS, Park JH, Lee BC. Surgical treatment of acute necrotizing pancreatitis. J Korean Surg Soc 1998;54:283–290.
3. Cooperman AM. Surgery and chronic pancreatitis. Surg Clin North Am 2001;81:431–455.
4. Haggard WD, Kirtley JA. Pancreatic calculi: a review of sixty-five operative and one hundred thirty-nine non-operative cases. Ann Surg 1939;109:809–826.
5. Planche NE, Palasciano G, Meullenet J, Laugier R, Sarles H. Effects of intravenous alcohol on pancreatic and biliary secretion in man. Dig Dis Sci 1982;27:449–453.
6. Ahn CS, Jang HJ, Kim SC, Han DJ. Surgical treatment of chronic pancreatitis. J Korean Surg Soc 1999;56:410–419.
7. Sakakibara A, Okumura N, Hayakawa T, Kanzaki M. Ultrastructural changes in the exocrine pancreas of experimental pancreatolithiasis in dogs. Am J Gastroenterol 1982;77:498–503.
8. Sakorafas GH, Farnell MB, Nagorney DM, Sarr MG. Surgical management of chronic pancreatitis at the Mayo Clinic. Surg Clin North Am 2001;81:457–465.
9. Ihse I, Borch K, Larsson J. Chronic pancreatitis: results of operations for relief of pain. World J Surg 1990;14:53–58.
10. Ammann RW, Akovbiantz A, Largiader F, Schueler G. Course and outcome of chronic pancreatitis: longitudinal study of a mixed medical-surgical series of 245 patients. Gastroenterology 1984;86(5 Pt 1):820–828.
11. Doubilet H, Mulholland JH. The surgical treatment of recurrent acute pancreatitis by endocholedochal sphincterotomy. Surg Gynecol Obstet 1948;86:295–306.
12. Doubilet H, Mulholland JH. Eight-year study of pancreatitis and sphincterotomy. J Am Med Assoc 1956;160:521–528.
13. Rösch T, Daniel S, Scholz M, et al. Endoscopic treatment of chronic pancreatitis: a multicenter study of 1000 patients with long-term follow-up. Endoscopy 2002;34:765–771.
14. Morgan DE, Smith JK, Hawkins K, Wilcox CM. Endoscopic stent therapy in advanced chronic pancreatitis: relationships between ductal changes, clinical response, and stent patency. Am J Gastroenterol 2003;98:821–826.
15. Gabbrielli A, Pandolfi M, Mutignani M, et al. Efficacy of main pancreatic-duct endoscopic drainage in patients with chronic pancreatitis, continuous pain, and dilated duct. Gastrointest Endosc 2005;61:576–581.
16. Eleftherladis N, Dinu F, Delhaye M, et al. Long-term outcome after pancreatic stenting in severe chronic pancreatitis. Endoscopy 2005;37:223–230.
17. Vitale GC, Cothron K, Vitale EA, et al. Role of pancreatic duct stenting in the treatment of chronic pancreatitis. Surg Endosc 2004;18:1431–1434.
18. Ponchon T, Bory RM, Hedelius F, et al. Endoscopic stenting for pain relief in chronic pancreatitis: results of a standardized protocol. Gastrointest Endosc 1995;42:452–456.
19. Link G. Pancreatostomy for chronic pancreatitis with calculi in the duct of Wirsung and diffuse calcinosis of the pancreatic parenchyma. Ann Surg 1953;138:287–288.
20. DuVal MK Jr. Caudal pancreatico-jejunostomy for chronic relapsing pancreatitis. Ann Surg 1954;140:775–785.
21. Puestow CB, Gillesby WJ. Retrograde surgical drainage of pancreas for chronic relapsing pancreatitis. AMA Arch Surg 1958;76:898–907.
22. Partington PF, Rochelle RE. Modified Puestow procedure for retrograde drainage of the pancreatic duct. Ann Surg 1960;152:1037–1043.
23. Priestley JT, Comfort MW, Radcliffe J. Total pancreatectomy for hyperinsulinism due to an islet-cell adenoma: survival and cure at sixteen months after operation presentation of metabolic studies. Ann Surg 1944;119:211–221.
24. Whipple AO. Radical surgery for certain cases of pancreatic fibrosis associated with calcareous deposits. Ann Surg 1946;124:991–1006.
25. Eliason EL, Welty RF. Pancreatic calculi. Ann Surg 1948;127:150–157.
26. Traverso LW, Longmire WP Jr. Preservation of the pylorus in pancreaticoduodenectomy. Surg Gynecol Obstet 1978;146:959–962.
27. Moosa AR. Surgical treatment of chronic pancreatitis: an overview. Br J Surg 1987;74:661–667.
28. Sakorafas GH, Farnell MB, Nagorney DM, Sarr MG, Rowland CM. Pancreatoduodenectomy for chronic pancreatitis: long-term results in 105 patients. Arch Surg 2000;135:517–523.
29. Jimenez RE, Fernandez-Del Castillo C, Rattner DW, Warshaw AL. Pylorus-preserving pancreaticoduodenectomy in the treatment of chronic pancreatitis. World J Surg 2003;27:1211–1216.
30. Gall FP, Mühe E, Gebhardt C. Results of partial and total pancreaticoduodenectomy in 117 patients with chronic pancreatitis. World J Surg 1981;5:269–275.
31. Russell RC, Theis BA. Pancreatoduodenectomy in the treatment of chronic pancreatitis. World J Surg 2003;27:1203–1210.
32. Vickers SM, Chan C, Heslin MJ, Bartolucci A, Aldrete JS. The role of pancreaticoduodenectomy in the treatment of severe chronic pancreatitis. Am Surg 1999;65:1108–1111.
33. Traverso LW. The pylorus preserving Whipple procedure for the treatment of chronic pancreatitis. Swiss Surg 2000;6:259–263.
34. McLaughlin EF, Harris JS. Total pancreatectomy for recurrent calcareous pancreatitis. Ann Surg 1952;136:1024–1030.
35. Braasch JW, Vito L, Nugent FW. Total pancreatectomy of end-stage chronic pancreatitis. Ann Surg 1978;188:317–322.
36. Cooper MJ, Williamson RC, Benjamin IS, et al. Total pancreatectomy for chronic pancreatitis. Br J Surg 1987;74:912–915.
37. Sawyer R, Frey CF. Is there still a role for distal pancreatectomy in surgery for chronic pancreatitis? Am J Surg 1994;168:6–9.
38. Bradley EL 3rd. Long-term results of pancreatojejunostomy in patients with chronic pancreatitis. Am J Surg 1987;153:207–213.
39. Mannell A, Adson MA, McIlrath DC, Ilstrup DM. Surgical management of chronic pancreatitis: long-term results in 141 patients. Br J Surg 1988;75:467–472.
40. Taylor RH, Bagley FH, Braasch JW, Warren KW. Ductal drainage or resection for chronic pancreatitis. Am J Surg 1981;141:28–33.
41. Izbicki JR, Bloechle C, Broering DC, Kuechler T, Broelsch CE. Longitudinal V-shaped excision of the ventral pancreas for small duct disease in severe chronic pancreatitis: prospective evaluation of a new surgical procedure. Ann Surg 1998;227:213–219.
42. Beger HG, Witte C, Krautzberger W, Bittner R. Experiences with duodenum-sparing pancreas head resection in chronic pancreatitis. Chirurg 1980;51:303–307.
43. Büchler MW, Friess H, Bittner R, et al. Duodenumpreserving pancreatic head resection: long-term results. J Gastrointest Surg 1997;1:13–19.
44. Beger HG, Schlosser W, Friess HM, Büchler MW. Duodenum-preserving head resection in chronic pancreatitis changes the natural course of the disease: a single-center 26-year experience. Ann Surg 1999;230:512–519.
45. Frey CF, Smith GJ. Description and rationale of a new operation for chronic pancreatitis. Pancreas 1987;2:701–707.
46. Frey CF, Amikura K. Local resection of the head of the pancreas combined with longitudinal pancreaticojejunostomy in the management of patients with chronic pancreatitis. Ann Surg 1994;220:492–504.
47. Gloor B, Friess H, Uhl W, Büchler MW. A modified technique of the Beger and Frey procedure in patients with chronic pancreatitis. Dig Surg 2001;18:21–25.
48. Klempa I, Spatny M, Menzel J, et al. Pancreatic function and quality of life after resection of the head of the pancreas in chronic pancreatitis: a prospective, randomized comparative study after duodenum preserving resection of the head of the pancreas versus Whipple's operation. Chirurg 1995;66:350–359.
49. Malka D, Hammel P, Sauvanet A, et al. Risk factors for diabetes mellitus in chronic pancreatitis. Gastroenterology 2000;119:1324–1332.
50. Andersen DK, Topazian MD. Pancreatic head excavation: a variation on the theme of duodenum-preserving pancreatic head resection. Arch Surg 2004;139:375–379.
51. Ho HS, Frey CF. The Frey procedure: local resection of pancreatic head combined with lateral pancreaticojejunostomy. Arch Surg 2001;136:1353–1358.
52. Ho HS, Frey CF. The Frey procedure: combined local resection of the head of the pancreas with longitudinal pancreaticojejunostomy. Operat Tech Gen Surg 2002;:153–167.
53. Farkas G, Leindler L, Daróczi M, Farkas G Jr. Organpreserving pancreatic head resection in chronic pancreatitis. Br J Surg 2003;90:29–32.
54. Farkas G, Leindler L, Daróczi M, Farkas G Jr. Prospective randomised comparison of organ-preserving pancreatic head resection with pylorus-preserving pancreaticoduodenectomy. Langenbecks Arch Surg 2006;391:338–342.
55. Büchler MW, Friess H, Müller MW, Wheatley AM, Beger HG. Randomized trial of duodenum-preserving pancreatic head resection versus pylorus-preserving Whipple in chronic pancreatitis. Am Surg 1995;169:65–69.
56. Strate T, Taherpour Z, Bloechle C, et al. Long-term followup of a randomized trial comparing the beger and frey procedures for patients suffering from chronic pancreatitis. Ann Surg 2005;241:591–598.
57. Köninger J, Seiler CM, Sauerland S, et al. Duodenumpreserving pancreatic head resection: a randomized controlled trial comparing the original Beger procedure with the Berne modification (ISRCTN No. 50638764). Surgery 2008;143:490–498.
58. Izbicki JR, Bloechle C, Broering DC, Knoefel WT, Kuechler T, Broelsch CE. Extended drainage versus resection in surgery for chronic pancreatitis: a prospective randomized trial comparing the longitudinal pancreaticojejunostomy combined with local pancreatic head excision with the pylorus-preserving pancreatoduodenectomy. Ann Surg 1998;228:771–779.
59. Izbicki JR, Bloechle C, Knoefel WT, Kuechler T, Binmoeller KF, Broelsch CE. Duodenum-preserving resection of the head of the pancreas in chronic pancreatitis: a prospective, randomized trial. Ann Surg 1995;221:350–358.
60. Riediger H, Adam U, Fischer E, et al. Long-term outcome after resection for chronic pancreatitis in 224 patients. J Gastrointest Surg 2007;11:949–959.
61. Izbicki JR, Bloechle C, Knoefel WT, et al. Drainage versus resection in surgical therapy of chronic pancreatitis of the head of the pancreas: a randomized study. Chirurg 1997;68:369–377.
62. Shrikhande SV, Kleeff J, Friess H, Büchler MW. Management of pain in small duct chronic pancreatitis. J Gastrointest Surg 2006;10:227–233.
63. Strate T, Bachmann K, Busch P, et al. Resection vs drainage in treatment of chronic pancreatitis: long-term results of a randomized trial. Gastroenterology 2008;134:1406–1411.
64. Müller MW, Friess H, Beger HG, et al. Gastric emptying following pylorus-preserving Whipple and duodenumpreserving pancreatic head resection in patients with chronic pancreatitis. Am J Surg 1997;173:257–263.
65. Müller MW, Friess H, Martin DJ, Hinz U, Dahmen R, Büchler MW. Long-term follow-up of a randomized clinical trial comparing Beger with pylorus-preserving Whipple procedure for chronic pancreatitis. Br J Surg 2008;95:350–356.
66. Najarian JS, Sutherland DE, Baumgartner D, et al. Total or near total pancreatectomy and islet autotransplantation for treatment of chronic pancreatitis. Ann Surg 1980;192:526–542.
67. Farney AC, Najarian JS, Nakhleh RE, et al. Autotransplantation of dispersed pancreatic islet tissue combined with total or near-total pancreatectomy for treatment of chronic pancreatitis. Surgery 1991;110:427–437.
68. Robertson RP, Lanz KJ, Sutherland DE, Kendall DM. Prevention of diabetes for up to 13 years by autoislet transplantation after pancreatectomy for chronic pancreatitis. Diabetes 2001;50:47–50.
69. Rastellini C. Donor and recipient selection in pancreatic islet transplantation. Curr Opin Organ Transplant 2002;7:196–202.
70. Rickels MR, Schutta MH, Markmann JF, Barker CF, Naji A, Teff KL. {beta}-cell function following human islet transplantation for type 1 diabetes. Diabetes 2005;54:100–106.
71. Shapiro AM, Ricordi C, Hering BJ, et al. International trial of the Edmonton protocol for islet transplantation. N Engl J Med 2006;355:1318–1330.
72. Robertson GS, Dennison AR, Johnson PR, London NJ. A review of pancreatic islet autotransplantation. Hepatogastroenterology 1998;45:226–235.
73. Ray BS, Console AD. Evaluation of total sympathectomy. Ann Surg 1949;130:652–671.
74. Rack FJ, Elkins CW. Experiences with vagotomy and sympathectomy in the treatment of chronic recurrent pancreatitis. AMA Arch Surg 1950;61:937–943.
75. Hammond B, Vitale GC, Rangnekar N, Vitale EA, Binford JC. Bilateral thoracoscopic splanchnicectomy for pain control in chronic pancreatitis. Am Surg 2004;70:546–549.
76. Buscher HC, Jansen JB, van Dongen R, Bleichrodt RP. Long-term results of bilateral thoracoscopic splanchnicectomy in patients with chronic pancreatitis. Br J Surg 2002;89:158–162.
77. Baghdadi S, Abbas MH, Albouz F, Ammori BJ. Systematic review of the role of thoracoscopic splanchnicectomy in palliating the pain of patients with chronic pancreatitis. Surg Endosc 2008;22:580–588.
78. Maher JW, Johlin FC, Pearson D. Thoracoscopic splanchnicectomy for chronic pancreatitis pain. Surgery 1996;120:603–609.
79. Howard TJ, Swofford JB, Wagner DL, Sherman S, Lehman GA. Quality of life after bilateral thoracoscopic splanchnicectomy: long-term evaluation in patients with chronic pancreatitis. J Gastrointest Surg 2002;6:845–852.
80. Lillemoe KD, Cameron JL, Kaufman HS, Yeo CJ, Pitt HA, Sauter PK. Chemical splanchnicectomy in patients with unresectable pancreatic cancer: a prospective randomized trial. Ann Surg 1993;217:447–455.
81. Gress F, Schmitt C, Sherman S, Ikenberry S, Lehman G. A prospective randomized comparison of endoscopic ultrasoundand computed tomography-guided celiac plexus block for managing chronic pancreatitis pain. Am J Gastroenterol 1999;94:900–905.