FLT3 돌연변이를 동반한 급성 골수성 백혈병의 최신 치료 전략
Recent Advances in Therapeutic Strategies for FLT3-Mutated Acute Myeloid Leukemia
Article information
Trans Abstract
FLT3 mutations occur in approximately 25% to 30% of newly diagnosed cases of acute myeloid leukemia (AML) and are typically associated with adverse prognoses characterized by a high risk of relapse. In recent years, the AML therapeutic landscape has been notably reshaped by the introduction of FLT3 inhibitors, including midostaurin, quizartinib, and gilteritinib. The European LeukemiaNet 2022 guidelines classify all FLT3-ITD-positive AML as intermediate risk, regardless of allelic ratios, thereby highlighting the importance of co-mutations and measurable residual disease (MRD). In fit patients (intensive chemotherapy eligible), the current standard therapy incorporates FLT3 inhibitor-based chemotherapy, allogeneic hematopoietic stem cell transplantation during the initial complete remission, and post-transplant maintenance. Long-term follow-up from the RATIFY trial confirmed durable survival benefits using midostaurin (10-year overall survival, 43.7%), whereas the QuANTUM-first study has provided evidence for the marked efficacy of quizartinib in patients with NPM1 and DNMT3A co-mutations. For unfit patients, although azacitidine plus venetoclax remains the standard therapy, early-phase studies evaluating FLT3 inhibitor-containing triplet regimens have revealed complete remission rates exceeding 80%. In addition, for cases of relapsed or refractory FLT3-mutated AML, gilteritinib has been established to provide a median overall survival of 9.3 months and serves as an effective bridge to transplantation, whereas venetoclax combinations can contribute to enhancing the length of remission. Recent advances in characterizing resistance mechanisms, including secondary TKD mutations and RAS/MAPK pathway activation, are contributing to the developments of next-generation covalent and multi-kinase FLT3 inhibitors, and it is anticipated that MRD-guided therapeutic adaptation and genomics-driven precision medicine will facilitate further refinement of future standards of the care.
서 론
급성 골수성 백혈병(acute myeloid leukemia, AML)은 조혈전구세포(hematopoietic progenitor cells)의 분화 장애와 무제한적인 증식을 특징으로 하는 이질적 혈액암이다. 이 중 FLT3유전자 변이는 새롭게 진단된 AML 환자의 약 25-30%에서 발견되는 가장 흔한 분자 이상 중 하나로 불량한 예후와 연관성이 잘 알려져 있다[1-3]. FLT3유전자 변이는 높은 백혈구 수, 짧은 무병 생존 기간, 조기 재발과 밀접한 관련이 있으며 최근 여러 FLT3 억제제의 도입으로 치료 전략이 크게 변화함에 따라 AML의 위험도 분류 역시 재정립되었다[1,2,4,5]. 본 논문에서는 주요 임상 연구 근거를 바탕으로 FLT3 변이 AML의 최신 치료 전략을 정리하고 국내 임상 환경에서 고려해야 할 실제적 적용점을 제시하고자 한다.
본 론
FLT3 변이의 생물학적 특성
FLT3수용체는 조혈전구세포 표면의 막관통형수용체 티로신키나아제로 정상적인 조혈 과정에서 세포 증식과 분화를 조절한다[6]. 가장 흔한 변이인 FLT3-internal tandem duplication (ITD)은 막인접부위(juxtamembrane region)에 반복 서열이 삽입되면서 발생하며 그 결과 리간드 결합 없이 수용체가 지속적으로 활성화된다. 이러한 활성화는 RAS/MAPK, PI3K/AKT, JAK/STAT5 등의 신호 전달 경로를 계속 자극하여 세포 생존과 증식을 우세하게 만들고 그 결과 항암제에 대한 반응이 떨어지며 미세 잔존 질환(measurable residual disease, MRD)이 지속되거나 증가하게 된다[6]. FLT3-tyrosine kinase domain (TKD) 변이는 활성 부위의 점 돌연변이로 수용체를 리간드가 없는 상태에서도 활성형으로 유지시킨다[6]. TKD 단독 변이는 ITD에 비해 예후가 반드시 불량한 것은 아니지만 특정 FLT3 억제제, 특히 quizartinib에 대한 내성과 연관되는 특징이 있으며 FLT3-ITD와는 생물학적 및 임상적 특성이 다른 독립된 분자 아형으로 이해되고 있다[7].
European LeukemiaNet 2022 위험 분류 체계의 변화
European LeukemiaNet (ELN) 2022 가이드라인은 FLT3-ITD 변이 AML의 위험 분류 방식을 크게 바꾸었다[1]. 과거에는 FLT3-ITD 대립유전자 비율(allelic ratio)이 중요한 예후 인자로 여겨졌지만 2022년 개정안에서는 더 이상 단독 위험 인자로 사용되지 않는다. 즉 불량한 예후의 유전자가 따로 동반되지 않다면 FLT3-ITD는 NPM1 변이 여부와 상관없이 모두 중간 위험군(intermediate risk)으로 분류된다[1]. 이러한 변화의 배경에는 대립유전자 비율 측정의 표준화 문제, FLT3 억제제 병용 치료의 도입으로 인한 예후 개선, MRD의 예후적 중요성 증가가 있다.
FLT3 억제제의 개발과 분류
FLT3 억제제는 수용체 결합 특성에 따라 제1형(type I)과 제2형(type II)으로 구분된다[7]. 제1형 억제제인 미도스타우린(midostaurin), 길테리티닙(gilteritinib), 크레놀라닙(crenolanib)은 활성형과 비활성형 수용체 모두에 결합하여 FLT3- ITD 및 TKD 변이를 모두 억제한다. 반면 제2형 억제제인 소라페닙(sorafenib), 퀴자르티닙(quizartinib)은 비활성형 수용체에만 결합하여 FLT3-ITD에는 효과적이나 TKD 변이에는 제한적이다[7]. 미도스타우린은 RATIFY 연구를 통해 생존 이득을 입증하며 FLT3 억제 시대의 서막을 열었으며[8] 이후 등장한 퀴자르티닙과 길테리티닙은 각각 신규 진단 환자 및 재발/불응 환자에서 임상적 유효성을 입증하면서 표준 치료로 자리잡았다[9,10].
FLT3 변이 급성 골수성 백혈병 신규 진단 환자의 치료 전략
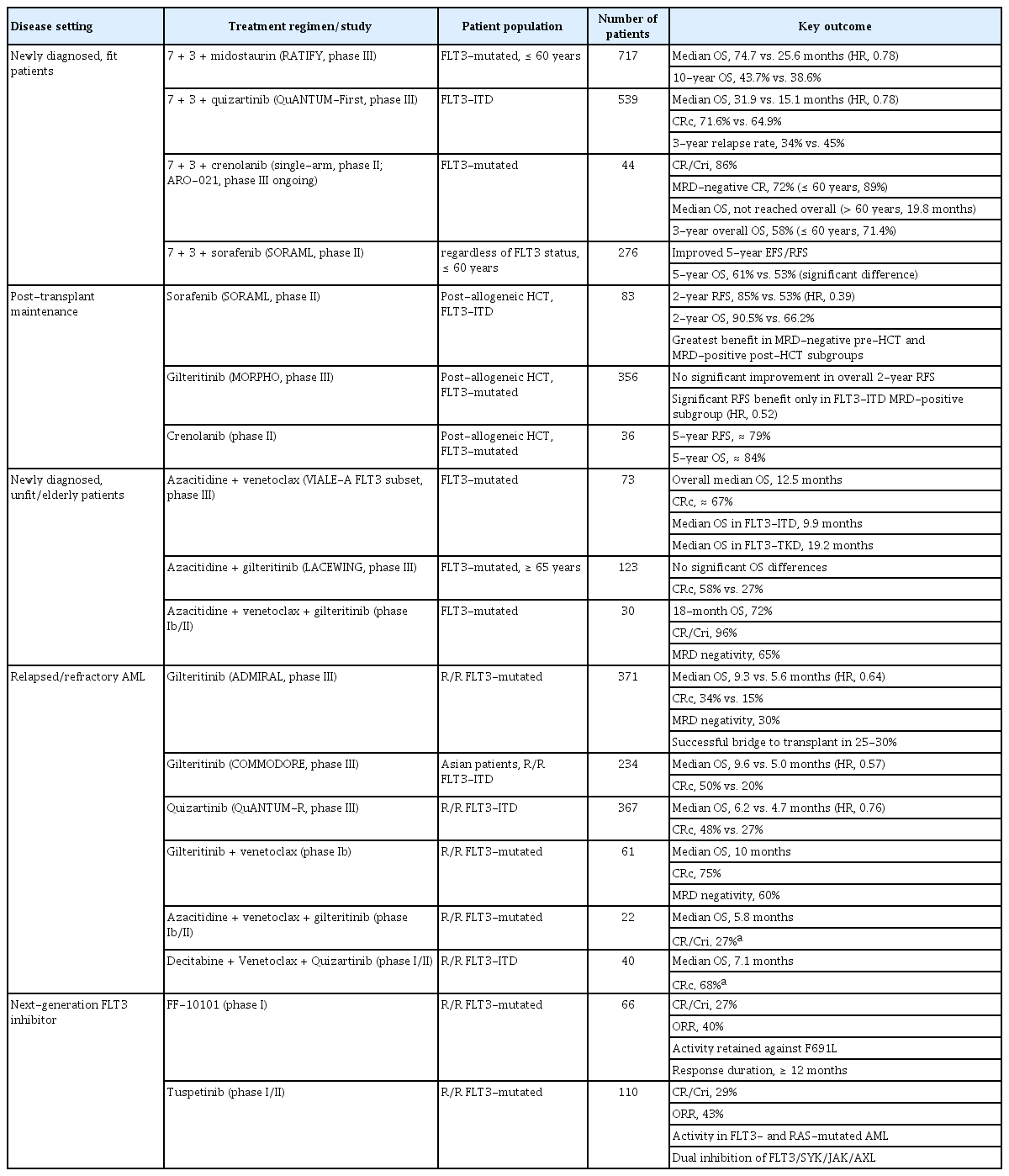
FLT3 변이 AML의 치료는 환자의 고강도 항암 치료 가능 여부에 따라 집중 치료군과 비집중 치료군으로 나뉜다. 각 임상 단계에서 사용되는 FLT3 억제제 병용 요법과 주요 임상시험 결과는 표 1에 요약하였으며 이후 절에서 각 치료군의 세부 데이터를 서술한다.
집중 치료가 가능한 환자(fit patients)
미도스타우린: FLT3 억제제 시대의 개막
집중 항암 요법 적합 환자에서는 표준 화학 요법(7 + 3)에 FLT3 억제제를 병용하는 것이 현재의 표준 치료이다. 대표적인 근거인 RATIFY 3상 연구는 미도스타우린(midostaurin)을 표준 화학 요법과 병용할 경우 생존율 향상을 입증하였다. 미도스타우린 병용군은 위약군 대비 4년 전체 생존율(51.4% vs. 44.3%; 위험도, 0.78; p= 0.009)에서 유의한 개선을 보였고 중앙 전체 생존 기간도 74.7개월(위약군, 25.6개월)로 향상을 보였다[8]. 2024년 American Society of Hematology (ASH)에서 발표된 10년 추적 결과는 이러한 생존 이득을 더욱 확고하게 하였는데, 10년 전체 생존율은 43.7%로 위약군(38.6%)에 비해 미도스타우린군이 생존율 향상이 장기 추적에서도 관찰되었다[11]. 또한 미도스타우린의 효과는 FLT3-ITD와 TKD 변이, allelic ratio와 무관하게 일관되게 관찰되었다[11].
퀴자르티닙: 2세대 FLT3 억제제의 효능
QuANTUM-First 연구는 퀴자르티닙(quizartinib)의 효능을 입증한 3상 임상시험으로 퀴자르티닙 병용군은 위약군 대비 중앙 전체 생존율(31.9개월 vs. 15.1개월; 위험도, 0.78; p= 0.032) 및 3년 누적 재발률(34% vs. 45%)에서 유의한 개선을 보였다[9]. 특히 하위 분석에서 FLT3-ITD, NPM1 및 DNMT3A triple genotype 돌연변이 환자에서 가장 큰 생존 이득(위험도, 0.47)이 관찰되었으며 NPM1 또는 DNMT3A 단독 변이, epigenetic regulator 변이 동반 시에도 효과적이었다[12]. 연령별 분석에서는 60세 미만 환자에서 퀴자르티닙의 효과가 더 뚜렷하였다[13].
퀴자르티닙과 미도스타우린의 직접 비교 연구는 아직 없으나 간접 치료 분석에서는 퀴자르티닙이 미도스타우린 대비 재발률 감소를 보였다(위험도, 0.42). 또한 실사용 증거(real-world evidence)에서는 퀴자르티닙이 더 높은 완전 관해율(85% vs. 73%)과 낮은 치료 중단율(5.0% vs. 25.5%)을 보였다[14,15]. 이는 퀴자르티닙이 미도스타우린 대비 재발 위험을 낮추고 더 깊고 지속적인 관해를 유도할 가능성을 시사하지만 이러한 결과는 간접 비교의 한계를 고려하여 신중히 해석되어야 하며 생존 개선 여부는 추가 추적 및 전향적 연구가 필요하다. 2025년 11월 30일 기준 현재 국내에서는 일차 치료로 표준 화학 요법(7 + 3)과 FLT3 억제제 병용 요법으로 미도스타우린만이 식품의약품안전처 허가를 받아 처방이 가능하나 건강보험심사평가원의 급여 승인은 아직 이루어지지 않은 상태이다.
동종 조혈모세포 이식 전략
FLT3 변이 AML 환자에서 1차 관해 시 동종 조혈모세포 이식은 무재발 생존율을 유의하게 향상시키고 전체 생존율 역시 개선한다. 이식 성공의 핵심 예측 인자는 MRD 음전 상태, 특히 FLT3-ITD 기반 MRD 음전 여부는 동종 조혈모세포 이식 후 재발 및 생존을 예측하는 중요한 독립 예후 인자로 보고되고 있다[16]. MRD 양성이 지속되는 고위험 환자에서는 이식 전 추가 공고 요법이나 FLT3 억제제를 포함한 가교 요법을 통해 질병의 부담을 최대한 감소시키는 전략이 고려되며 일부 연구에서 안정성과 잠재적 유효성이 보고되고 있다[17].
이식 후 유지 요법
이식 후 유지 요법(post-transplant maintenance)은 FLT3 변이 AML 환자의 재발 방지를 위한 중요한 치료 방법이다. SORMAIN 연구에서는 소라페닙(sorafenib) 유지 요법을 사용한 환자들의 2년 무재발 생존율은 85%로 위약군의 53%에 비해 재발과 사망 위험을 크게 줄였다(위험도, 0.25; p= 0.002) [18]. MORPHO 연구에서는 FLT3-ITD 변이가 있고 이식 전후로 MRD 양성 환자군에서만 길테리티닙(gilteritinib) 유지 요법이 무재발 생존율을 유의하게 개선하였고(위험도, 0.52; p= 0.0065) MRD 음전율도 증가시켰다[19].
이 두 연구 모두 FLT3 변이 AML 환자에서 이식 후 유지 요법의 효과를 확인하였으며 특히 MRD 양성 환자군에서 생존율 향상이 두드러져 고위험 AML 환자의 맞춤 치료 전략에 중요한 근거가 된다. ELN 2022 및 National Comprehensive Cancer Network (NCCN) 가이드라인은 소라페닙 또는 길테리티닙 유지 요법을 권고하나 미도스타우린 유지 요법은 RATIFY 10년 추적 결과에서 전체 생존율 개선 없이 오히려 치료 관련 사망이 증가하여 표준 유지 요법으로는 권장되지 않지만 일부 유럽 국가에서는 여전히 승인되어 사용 중이다[11]. 2025년 11월 30일 기준 현재 국내에서는 FLT3 억제제의 이식 후 유지 요법 적응증에 대해 식품의약품안전처 허가 또는 건강보험심사평가원 급여 승인은 이루어지지 않은 상태이다.
집중 치료가 어려운 환자(unfit patients)
저메틸화제와 베네토클락스 병용 요법
아자시티딘과 베네토클락스(azacitidine + venetoclax) 병용 요법은 고령 환자 또는 동반 질환으로 고강도 항암 요법이 어려운 AML 환자에서 표준 치료로 자리 잡았다. FLT3 변이 환자를 대상으로 한 하위 분석에서는 완전 관해/불완전 혈액학적 회복을 동반한 완전 관해율(complete remission/complete remission with incomplete hematologic recovery, CR/CRi) 67%, 중앙 전체 생존 기간12.5개월로 의미 있는 결과를 보였다[20]. 그러나 FLT3-ITD 변이 그룹에서는 조기 재발이 빈번하게 관찰되는데 이는 FLT3-ITD 신호전달이 항고사 단백질(anti-apoptotic protein)인 MCL-1 및 BCL-xL 발현을 유도하여 베네토클락스에 대한 내성을 유발하기 때문으로 해석된다[21].
저메틸화제-FLT3 억제제 2제 병용: 제한적 효과
FLT3 억제제를 추가한 2제 병용 요법이 시도되었으나 결과는 실망스러웠다. LACEWING 3상 연구에서 아자시티딘과 길테리티닙 2제 요법은 58%의 완전 관해율에도 불구하고 아자시티딘 단독 요법 대비 전체 생존율 개선이 없어 조기 종료되었다[22]. 이는 저메틸화제와 FLT3 억제제 2제 병용만으로는 베네토클락스의 항세포자멸 경로 억제의 이점을 대체하기 어렵다는 점을 시사한다.
3제 병용 요법: 미래의 표준 치료?
최근 3제 병용 요법(저메틸화제 + 베네토클락스 + FLT3 억제제)이 새로운 치료 선택지로 부상하고 있으며 초기 결과는 유망하다. 후향적 분석에서 3제 병용군은 2제 병용군 대비 완전 관해율(67% vs. 32%), CR/CRi 비율(93% vs. 70%), 중앙 전체 생존율(미도달 vs. 9.5개월) 모두에서 우월한 결과를 보였다[23]. 전향적 연구에서도 아자시티딘 + 베네토클락스 + 길테리티닙 3제 병용 요법(n = 30)은 복합 완전 관해 96% (완전 관해, 90%), 18개월 전체 생존율 72%를 달성하였다[24]. 다만 골수 억제와 감염 위험이 높아 용량 조절 등 독성 완화 전략이 필수적이다[23]. 3제 병용 요법은 현재 제2상 임상시험 단계에 있으며 향후 비집중 치료에 적합한 환자들의 표준 치료로 발전할 가능성이 높다.
미세 잔존 질환 기반 치료 전략
MRD는 FLT3 변이 AML에서 가장 강력한 예후 인자로 부상하였다. 그러나 관해 유도 항암 요법 후 MRD 음성이라 하더라도 FLT3 변이 AML의 내재적 재발 위험을 완전히 상쇄하지는 못하므로 현재의 표준 치료는 첫 번째 완전 관해(CR1)에서 동종 조혈모세포 이식을 시행하는 것이다. 공고 요법 후 MRD 평가는 가교 요법의 필요성 판단에 활용되며 이식 직전 FLT3-ITD를 이용한 MRD는 이식 후 예후 예측, 전처치 항암제 강도 결정 및 유지 요법 계획 수립에 도움을 준다[17]. 또한 이식 후 정기적 MRD 모니터링은 선제적 개입에 활용되며 MRD가 재출현할 경우 면역 억제제 조절, FLT3 억제제 재투여 및 2차 이식 등의 전략이 고려된다[25]. MRD 맞춤 적응 치료(MRD-guided adaptive therapy)는 고정된 치료 스케줄을 벗어나 개별 환자의 질병 동태에 따라 치료를 조절함으로써 불필요한 독성을 줄이고 치료 효과를 극대화하는 정밀의학의 중요한 전략으로 부상하고 있다[25,26].
재발/불응성 환자의 치료 전략
FLT3 억제제의 도입으로 AML의 치료 성적은 눈에 띄게 개선되었다. 그러나 재발/불응성(relapsed/refractory, R/R) FLT3 변이 AML은 여전히 예후가 불량한 아형으로 남아 있다. 집중 항암 요법 이후 재발한 환자의 중앙 생존 기간은 6개월 미만으로 기존의 구제 화학 요법만으로는 의미 있는 장기 생존을 기대하기 어렵다. 이러한 배경에서 FLT3 억제제, 특히 길테리티닙은 R/R FLT3 변이 AML 치료의 중심축으로 자리 매김하고 있다[10].
FLT3 억제제 단독 요법
길테리티닙(gilteritinib)은 활성형과 비활성형 FLT3수용체 모두에 결합하는 type I 억제제로 R/R FLT3 변이 AML에서 탁월한 효능을 입증하였다. ADMIRAL 3상 연구에서 길테리티닙 단독 요법은 기존 구제 화학 요법 대비 중앙 전체 생존 기간(9.3개월 vs. 5.6개월; 위험도, 0.64; p< 0.001) 완전 관해 및 혈액학적 회복을 동반한 완전 관해(CR/CRh) 비율(34.0% vs. 15.3%; p= 0.0001)에서 우월한 결과를 보였다[10]. 또한 길테리티닙은 MRD 음전율이 25-30%에 달했으며 동종 조혈모세포 이식으로의 가교 성공률 또한 25-30%를 보여주었다. 장기 추적에서 이식 후 길테리티닙 유지 요법을 시행받은 환자군의 2년 전체 생존율은 약 60%에 달하였다[27]. COMMODORE 3상 연구에서는 등록된 234명의 환자 중 201명(85.9%)이 아시아인이었으며 길테르티닙 단독 요법과 구제 화학 요법을 비교하였다[28]. 중앙 생존 기간은 길테르티닙군이 9.6개월, 구제 화학 요법군이 5.0개월이었고 복합 완전 관해율은 각각 50.0%와 20.3%로 보고되었다[28]. 이러한 결과는 ADMIRAL 연구와 유사한 생존 이득을 시사한다.
한편 퀴자르티닙도 R/R FLT3-ITD 변이 AML 환자 367명을 대상으로 단독 요법의 효용성을 평가한 QuANTUM-R 3상 연구가 진행되었으며 중앙 생존 기간은 퀴자르티닙 6.2개월, 구제 화학 요법 4.7개월로 나타났다(위험도, 0.76; 95% confidence interval, 0.58-0.98; p= 0.02) [29]. 주요 부작용은 QTc 연장과 골수 억제가 보고되었으나 대부분 관리가 가능한 수준이었다[29]. 그러나 퀴자르티닙은 미국 식품의약국(United States Food and Drug Administration, FDA) 승인을 받지 못해 국내에도 아직 허가가 이루어지지 않은 상태이다. 2025년 11월 기준 국내에서는 R/R FLT3-ITD 변이 AML 환자에 대해 길테리티닙만이 식품의약품안전처의 승인하에 단독 요법으로 사용되고 있다.
내성 극복 전략과 차세대 억제제
AML 환자에서 FLT3 억제제의 도입은 치료 결과를 전반적으로 향상시켰으나 치료 후 재발은 여전히 빈번하다. 내성 발생은 단일 기전이 아닌, 약물 결합 부위의 변이, 하위 신호 경로의 재활성화, 골수 미세환경의 보호 효과가 복합적으로 작용한 결과이다[30]. 첫째, on-target 내성 기전으로는 약물 결합 부위의 변이가 대표적이며 특히 FLT3-TKD 내의 D835, F691L 변이가 억제제의 결합력을 감소시켜 내성을 일으킨다[30]. 둘째, off-target 내성에는 RAS/MAPK, PI3K/AKT 등 하위 신호 경로의 보상적 재활성화가 포함되며 이는 FLT3 비의존성 생존 신호를 활성화하여 약물의 효과를 회피하게 만든다[30]. 셋째, 골수의 미세환경의 보호 효과도 내성 기전에 중요한 역할을 한다. 골수의 stromal niche는 CXCL12/CXCR4 축을 통해 백혈병 세포를 약제 독성으로부터 보호하며 이로 인한 환경적 내성이 발생한다. 따라서 FLT3 억제제 단독 요법만으로는 장기적인 질병 통제를 유지하기 어렵고 다중 신호를 동시에 억제하는 병용 요법이 내성 극복의 핵심 전략으로 부상하고 있다[30].
베네토클락스 기반 병용 전략
R/R FLT3 변이 AML에서 가장 주목받는 병용 전략은 길테리티닙과 베네토클락스의 조합이다. FLT3 억제는 백혈병 세포의 BCL-2 의존성을 회복시켜 베네토클락스의 감수성을 높이며 두 약제의 병용은 세포자멸 경로를 증폭시켜 잔존 클론 제거에 효과적이다[31]. Ib상 연구에서 길테리티닙과 베네토클락스의 병용 요법은 R/R FLT3 변이 AML 환자 61명 중 75%에서 복합 완전 관해를 달성하였고 복합 완전 관해에 도달한 환자 중 MRD 음전율 60%, 중앙 생존 기간은 10개월을 기록하였다[32]. 이러한 결과는 FLT3 억제제 단독의 반응 소실을 지연시키며 일부 환자에서 동종 조혈모세포 이식으로의 연결을 가능하게 하였다. 주요 독성은 골수 억제와 감염이지만 베네토클락스의 14일 단축 요법과 조기 골수 평가를 통해 관리 가능하다. Ib/II상 퀴자르티닙과 베네토클락스 병용 연구가 진행 중이며(NCT03735875) 초기 데이터는 길테르티닙과 베네토클락스 병용 연구와 유사한 효능을 시사한다[33].
3제 병용 요법
또 다른 접근은 3제 병용 요법(저메틸화제 + 베네토클락스 + FLT3억제제)으로 R/R 환자에서 유망한 치료 전략으로 평가되고 있다. 전향적 Ib/II상 연구에서 아자시티딘 + 베네토클락스 + 길테리티닙의 병용은 복합 완전 관해율 27%, 중앙 생존율 5.8개월을 보였다[28]. 또한 데시타빈 + 베네토클락스 + 퀴자르티닙(I/II상)은 복합 완전 관해율 68%, 중앙 전체 생존 기간 7.1개월의 결과를 보고하였다[34]. 이러한 초기 결과는 R/R 환자에서도 3제 병용 전략의 임상적 확장 가능성을 보여준다.
후성 유전 및 신호전달 경로 표적 병용
FLT3 억제제는 epigenetic 또는 signal pathway 기반 약제와의 병용에서도 시너지 효과를 보인다[35]. Menin 억제제인 revumenib과 ziftomenib은 NPM1 변이나 MLL 재배열이 동반된 FLT3 변이 AML에서 분화 유도를 촉진하며 FLT3 억제제와 병용 시 백혈병줄기세포(leukemia stem cell)의 생존 신호를 억제한다[35]. 또한 IDH 억제제인 ivosidenib 또는 enasidenib이나 MEK 억제제인 trametinib과 binimetinib과의 병용은 각각 대사적 및 신호전달 수준에서의 보완 억제를 유도하며 내성 출현 이전에 클론 진화를 억제하는 치료 전략(evolution-suppressive therapy)으로 평가되고 있다[36,37].
차세대 FLT3 억제제의 개발
기존 FLT3 억제제의 한계를 극복하기 위한 차세대 억제제들이 개발되고 있다. 크레놀라닙(crenolanib)은 활성형 FLT3에 높은 친화도를 가진 type I 억제제로 7 + 3 기반 집중 항암 요법과의 병용 phase II 연구에서 성인 신규 진단 FLT3 변이 AML 환자(n = 44)에서 CR/CRi 86%, 3년 전체 생존율 58% (60세 이하 71%)라는 양호한 장기 생존 결과를 보였다[38]. 이러한 결과를 바탕으로 현재 크레놀라닙과 미도스타우린을 비교하는 ARO-021 phase III 무작위 대조 연구가 진행 중이다.
FF-10101은 FLT3의 Cys695 잔기에 비가역적으로 결합하는 공유결합 억제제로 F691L gatekeeper 변이에서도 활성을 보인다. 1상 임상시험에서 R/R AML 66명 중 CR/CRi 27%, 전체 반응률은 40%를 달성하였으며 일부 환자에서 12개월 이상 지속 반응이 확인되었다[39].
투스페티닙(tuspetinib)은 FLT3뿐 아니라 SYK, JAK, AXL 신호를 동시 억제하는 다중 키나아제 억제제로 R/R AML 환자를 대상으로 한 1/2상 연구에서 CR/CRi 29%, 전체 반응률은 43%를 기록하였다. 특히 FLT3 또는 RAS 변이 환자에서 더 높은 반응률을 보였으며 venetoclax 병용 시 항종양 활성이 강화되었다[40].
결 론
FLT3 억제제의 발전은 AML 치료의 새로운 전환점을 열었다. 1세대 억제제인 미도스타우린이 생존율 향상의 근거를 마련하였고 퀴자르티닙과 길테리티닙은 질병 단계에 따른 표적 치료의 정밀화를 가능하게 하였다. 그러나 내성과 재발은 여전히 극복해야 할 과제이며 베네토클락스 기반 병용 요법과 차세대 FLT3 억제제의 개발은 이를 해결하기 위한 중요한 진전으로 평가된다. 향후 치료의 핵심은 변이 스펙트럼, 동반 유전자 변이, MRD 및 클론 진화의 동태를 반영한 맞춤형 치료 조정에 있다.
다만 FLT3 억제제는 고가의 표적 치료제로 현재 국내에서는 허가 및 급여 적용에 제한이 있어 실제 임상 접근성에 제약이 존재한다. 향후 이러한 제도적, 경제적 장벽을 완화하고 근거 기반의 적절한 급여 체계가 마련된다면 FLT3 변이 AML은 더 이상 재발이 불가피한 치명적 질환이 아니라 장기 생존이 가능한 관리 질환으로 전환될 것으로 기대된다.
Notes
CONFLICTS OF INTEREST
No potential conflict of interest relevant to this article was reported.
FUNDING
None.
AUTHOR CONTRIBUTIONS
MK and JSA contributed to the conceptualization, data interpretation, and writing the manuscript.
ACKNOWLEDGEMENTS
The authors thank the staff of Chonnam National University Hwasun Hospital.