원위신세관산증이 선행한 전신홍반루푸스
- 강진영, 강종완, 김지훈, 진미경, 임철현, 남언정, 강영모
Systemic Lupus Erythematosus Preceded by Distal Renal Tubular Acidosis
- Jin Young Kang, Jong Wan Kang, Ji Hun Kim, Mi-Kyung Jin, Churl Hyun Im, Eon Jeong Nam, Young Mo Kang
- Received August 23, 2010; Revised September 1, 2010; Accepted October 14, 2010;
- Abstract
-
원위신세관산증은 세관내 산 분비의 저하로 소변의 산성화 장애와 전신적인 산혈증 및 저칼륨혈증을 특징으로 하는 질환이다. 루푸스를 비롯한 자가면역질환에 동반되는 원위신세관산증은 대부분 자가면역질환 발현 후에 나타나며 원위신세관산증이 먼저 발생하고 자가면역질환이 수개월에서 수년 후 발생하는 경우는 세계적으로 매우 드물게 보고되어 있다. 저자들은 원위신세관산증으로 진단되고 21년 후에 전형적인 루푸스 임상 증상들이 나타난 증례를 경험하였기에 문헌고찰과 함께 보고하는 바이다.
- Abstract
-
Distal renal tubular acidosis (RTA) is characterized by a decreased net H+ secretion in the collecting tubules, which results in a failure of urine acidification and results in metabolic acidosis, hypokalemia, and nephrocalcinosis. The acquired form of distal RTA is associated with tubulointerstitial involvement of immune-mediated disorders such as Sjogren’s syndrome and systemic lupus erythematosus (SLE). Only a few case reports have indicated that distal RTA precedes SLE by months to years. We present a 39-year-old woman who had manifestations of distal RTA for 21 years before the development of overt symptoms of SLE. (Korean J Med 2011;81:533-536)
- 서 론
- 서 론
원위신세관산증은 수소이온 배설 장애에 따른 요의 산성화 실패, 고염소혈증성 대사성산증, 저칼륨혈증, 그리고 신장석회증을 특징으로 한다. 원위신세관산증은 원인에 따라 일차성과 이차성으로 분류되며 쇼그렌증후군 및 전신홍반루푸스(이하 루푸스)를 포함하는 자가면역질환은 이차성의 중요한 원인질환이다[1]. 루푸스에 원위신세관산증이 동반되는 경우는 흔치 않으며 대부분 루푸스 신장염에 의한 증상으로 나타난다[2]. 하지만 원위신세관산증이 발생한 후 수개월에서 수년 후 루푸스가 진단된 경우도 드물게 보고되어 있다[3-6]. 저자들은 21년 동안 원위신세관산증으로 인한 전해질 이상 소견을 나타낸 환자에서 루푸스의 전형적인 임상 증상이 확인된 증례를 경험하였기에 보고하는 바이다.
- 증 례
- 증 례
환 자: 39세 여자주 소: 전신 쇠약감과 14일간의 복통가족력: 특이사항 없었다.과거력 및 현병력: 18세부터 간헐적으로 갑자기 잘 걷지 못하다가 수 시간 후에 다시 걸을 수 있게 되는 현상을 경험하였으며, 21세 때 성장 부전 소견 및 양 하지 쇠약감이 지속되어 원위신세관산증 및 골연화증으로 진단받고 중탄산염 및 칼륨을 복용하며 지내왔다. 내원 2주 전부터 전신 쇠약감, 열감, 근육통 및 복통이 지속되어 응급실로 내원하였다.이학적 소견: 내원 당시 혈압은 113/69 mmHg, 맥박수는 138회/분, 호흡수는 24회/분, 체온은 38.2℃였다. 신장은 137 cm였고, 체중은 34 kg였다. 복부 진찰에 압통이 있었으며 경도의 복부 팽만과 이동둔탁음 소견이 있었다. 그 외 특이한 소견은 없었다.검사실 소견: 말초혈액 검사에서 백혈구 15,070/mm3 (중성구 86.9% 및 림프구 9%), 혈색소 10.2 g/dL, 그리고 혈소판 435,000/ mm3이었으며, 적혈구침강속도 120 mm/hr, C-반응 단백 9.45 mg/dL이었다. 전해질 검사에 나트륨 129 mmol/L, 칼륨 1.9 mmol/L, 염소 160 mmol/L, 칼슘 9.8 mg/dL, 인 1.2 mg/dL, 그리고 요산 7.9 mg/dL였다. 생화학 검사에서 혈액요소질소 50.6 mg/dL, 크레아티닌 3.9 mg/dL, 총 단백 8.3 g/dL, 알부민 3.0 g/dL, AST 19 U/L, ALT 12 U/L, 젖산탈수소효소 652.5 IU/L, 아밀라아제 1,153 U/L, 리파제 5,354 U/L, 크레아틴인산활성효소 54 IU/L, 미오글로빈 422 ng/mL, 그리고 알돌라아제 5.3 U/L이었다. 동맥혈 가스 분석은 pH 7.28, pCO2 10.9 mmHg, pO2 128.3 mmHg, HCO3- 10.9 mmol/L, 음이온 차이 16.6 mmol/L, 그리고 산소포화도 99.1%이었다. 요검사에서 pH 8.0, 비중 1.015, 단백 2+, 적혈구 3-5/HPF, 백혈구 6-10/HPF이었다. 24시간 요검사에서 단백 1,207 mg, 칼슘 220 mg, 인 315 mg, 나트륨 83 mmol/L, 그리고 칼륨 13.2 mmol/L이었으며, 크레아티닌 청소율은 14.4 mL/min/1.73 m2이었다. 갑상선 기능검사는 정상이었다. 면역학적 검사에서 항핵항체 1:320 (homogenous pattern), 항이중가닥DNA 항체 24.3 IU/mL (정상범위: 0-7 IU/mL), 항Ro 항체 243.61 AAU/mL (정상범위: < 150 AAU/mL)로 상승되어 있었으나, 항La 항체, 류마티스인자, 항CCP 항체, 항중성구세포질 항체, 루푸스 항응고인자, 항cardiolipin 항체, 항RNP 항체, 그리고 항Sm 항체는 모두 음성이었다. 혈청 C3 48.6 mg/dL (정상범위: 90-180 mg/dL), C4 16.1 mg/dL (정상범위: 10-40 mg/dL)였다. 복수 천자 소견에서 세포수 7,200/μL (다형핵 호중구 80% 및 림프구 20%), 포도당 76 mg/dL, 단백 6 g/dL, 젖산탈수소효소 1,033.5 U/L (혈청/ 복수 비 0.63), 아데노신탈아미노효소 75.1 IU/L, 알부민 2.4 g/dL (혈청-복수 알부민 차이 0.6 g/dL)였다.방사선학적 소견: 흉부 X-선상 특이 소견 없었으며 단순 복부 X-선상 마비성 장폐색증 소견이 보였다. 복부전산화단층촬영에 복강 내 중등도의 복수가 있었으며, 양측 신장 수질에 석회화 소견이 보였다(Fig. 1). 골밀도 검사상 1번 요추 부위에 T 점수는 -2.4이었다. 심전도 상 전해질 이상에 따른 변화나 심장막염의 소견은 관찰되지 않았으며, 심초음파 상 특이 소견은 보이지 않았다.치료 및 경과: 루푸스에 동반된 신장염, 췌장염 및 복막염으로 진단되었으며, 금식 및 총정맥영양법과 함께 전해질을 교정하면서 메틸프레드니솔론(0.5 mg/kg)을 정맥투여하였다. 이후 열은 더 이상 발생하지 않았고, 치료 시작 40일에는 적혈구침강속도 및 C-반응 단백이 정상화되었으며, 아밀라아제 24 U/L, 리파제 201 U/L, C3 107.4 mg/dL 및 C4 26 mg/dL로 호전되었다. 전해질도 나트륨 145 mmol/L, 칼륨 4.7 mmol/L, 염소 112.5 mmol/L, 칼슘 8.4 mg/dL, 그리고 인 2.9 mg/dL로 호전되었고, 동맥혈 가스 pH 7.309, 24시간 요단백 400 mg, 그리고 크레아티닌 청소율 29 mL/min/1.73 m2로 회복되었으며 퇴원 후 현재 외래에서 추적관찰 중이다.
- 고 찰
- 고 찰
원위신세관산증의 원인은 원발성과 속발성으로 나눌 수 있고, 속발성은 Marfan 증후군 및 Ehlers-Danlos 증후군과 같은 유전성 질환[7], 원발성 부갑상선 기능항진증, 수질해면체신, 원발성 고칼슘뇨증과 같은 대사성 질환, amphotericin B, toluene, lithium 등의 약물에 의해 발병하며 쇼그렌증후군, 류마티스관절염, 그리고 루푸스와 같은 자가면역질환 의해서도 유발될 수 있다[8]. 루푸스나 쇼그렌증후군에서는 요세관간질 신장염을 동반하는 경우가 많으며 이것이 원위신세관산증의 중요 원인으로 추정되고 있다[2,9]. 본 증례에서는 항Ro 항체 양성 소견을 보였으나 입 마름, 눈 마름 증상이 전혀 없어 쇼그렌증후군은 배제할 수 있었다. 원위신세관산증의 병인 기전은 신세관의 H+-ATPase, anion exchange 1 (AE1), carbonic anhydrase (CA) II의 돌연변이나 림프구의 세뇨관 주위조직 침윤, 세뇨관의 면역 복합체의 침윤과 고감마글로불린혈증 등이 관련되어 있는 것으로 알려져 있으며, 이로 인해 요세관간질에 있는 효소의 기능장애가 일어남으로써 적절한 요 산성화가 유지되지 못하게 된다[1,10].루푸스에 있어 신장염은 비교적 흔한 증상으로써 사구체 신장염이 주요 소견이지만 요세관간질 침범도 빈번히 동반되는데[11] 신세관 장애를 가진 루푸스 환자의 약 50-70%에서 신세관 위축, 간질 침착 및 섬유화 등이 동반된다고 알려져 있다[12]. 루푸스의 급성 악화시기에는 60%의 환자에서 원위신세관 기능장애가 관찰되었다[2]. 일부 보고에 따르면, 루푸스에서 신세관 기능장애가 신세관산증의 임상증상 없이도 동반될 수 있으며[13] 약 20-30% 정도에서는 산혈증을 동반한 완전 원위신세관산증을 나타낸다는 보고도 있다[14]. 원위신세관산증이 동반된 루푸스에서 요세관간질 질환의 활성도나 사구체 질환이 원위신세관산증과 상관관계를 나타내지는 않았다[2,15]. 또한, 원위신세관산증은 루푸스의 특징적인 증상이 발생하기 수개월에서 수년 먼저 발생한 경우도 드물지만, 보고되어 왔다[3-6]. Ter Meulen 등[5]은 원위신세관산증에 의한 심한 저칼륨혈증 및 마비증이 발생한 후 6년 뒤에 루푸스가 동반된 증례를 보고하였다. 이들 보고에서는 원위신세관산증이 루푸스의 첫 번째 증상으로 나타난 것으로 설명하였다. 즉, 무증상 루푸스 기간에 먼저 신장에서 염증이 진행되어 원위신세관산증이 발생하였으며, 수개월에서 수년 지속 후 다른 특징적인 증상이 발생하면서 루푸스가 진단되었다고 추정하였다. 본 증례는 21년간 원위신세관산증 소견을 보이다가 루푸스의 다른 임상증상이 나타난 경우로 원위신세관산증이 루푸스의 첫번째 증상이었다고 생각하기는 시간 간격이 너무 긴 편이나, 발병 당시 루푸스에 의한 요세관간질 염증으로 원위신세관산증이 발생한 후 적절한 치료가 없었기 때문에 루푸스가 호전된 후에도 비가역적인 손상이 지속되었을 가능성도 있다.다른 관점에서 볼 때, 공통의 발병기전에 의한 루푸스와 원위신세관산증이 발병하였을 가능성을 생각할 수 있다. 루푸스 발병에 Epstein-Barr virus (EBV)가 관련되었을 가능성이 제시되어 왔으며, 루푸스 환자에서 EBV의 감염률이 높은 것으로 보고되었다[16,17]. 뿐만 아니라, EBV 감염은 림프구 침윤을 동반한 간질성 신장염을 유발하기도 한다[17]. 이는 바이러스 감염이 루푸스와 원위신세관산증의 발병에 공통의 유발 인자가 될 수 있다는 점을 시사한다. 또 다른 가능성으로 원위신세관산증이 지속됨으로써 이차적으로 루푸스가 발병하였을 가능성도 고려할 수 있으나 이에 대한 근거자료가 없어 앞으로 추가적인 연구가 필요할 것이다.본 증례에서는 루푸스가 발병하면서 원위신세관산증에 의한 기존의 전해질 이상이 악화되었다가 당질코르티코이드 치료 후 호전되어 루푸스 발병 이전 상태로 회복되었다. 이는 기존의 원위신세관산증에 더해 루프스 신장염이 발생하면서 원위신세관산증의 소견이 급격하게 악화되었다고 추정할 수 있다. 즉, 루푸스 활성도의 증가로 인해 신세관 기능장애가 악화되었고, 원위신세관산증에 의한 전해질 이상이 더 심해질 수 있었을 것이다[2]. 그리고 요세관간질 염증에 의한 세관의 손상이 원위신세관 기능을 악화시켰거나 루푸스에 의해 생산된 항CA II 항체가 원위신세관산증을 악화시켰을 가능성도 고려할 수 있다[18,19]. PL/J 마우스에서 CA II에 대한 항체 형성을 유발시키면 침샘과 신장에서 림프구와 형질세포의 침윤을 관찰할 수 있었으며, 소변의 산성화 장애가 생겼다는 보고가 있어 이를 뒷받침한다[18]. 루푸스 환자에서 당질코르티코이드에 의해 원위신세관산증이 회복되는 경우도 보고되어 있으나[12], 오래 지속된 원위신세관산증의 경우 루푸스 진단 후 당질코르티코이드로 치료하였으나 원위신세관산증의 호전이 되지 않았다는 보고도 있다[5]. 본 증례 경우에도 당질코르티코이드로 치료하였으나 요산성화 장애가 루푸스 발병이전 상태로만 회복되었으며, 이는 루푸스 활동성 증가로 인한 원위신세관산증의 악화는 회복되었지만 요세관간질의 미만성 비가역적인 손상이 남아있기 때문으로 추정된다.본 증례는 원위신세관산증이 시작된 후 루푸스의 발병까지의 기간이 현재까지 세계적으로 보고된 증례 가운데 가장 긴 21년에 이르며 원위신세관산증과 루푸스간의 인과 관계에 대해서는 명확히 규명되지 않았기 때문에 향후 이에 대한 연구가 필요할 것이다.
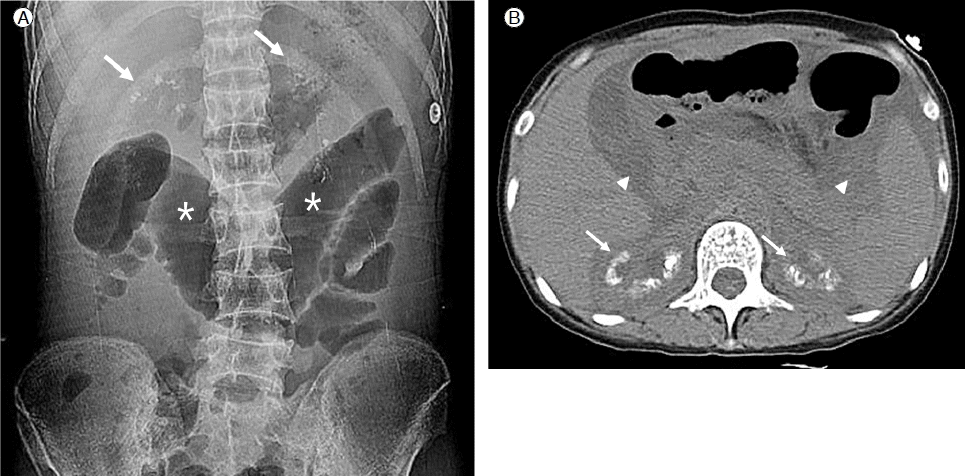
Figure 1.
A simple radiograph (A) and a computed tomography scan (B) of the abdomen showing bilateral nephrocalcinosis (arrow), ascites (arrow head), and paralytic ileus (asterisks).
- References
- References
REFERENCES
1. Rodríguez Soriano J. Renal tubular acidosis: the clinical entity. J Am Soc Nephrol 2002;13:2160–2170.
[Article] [PubMed]2. Kozeny GA, Barr W, Bansal VK, et al. Occurrence of renal tubular dysfunction in lupus nephritis. Arch Intern Med 1987;147:891–895.
[Article] [PubMed]3. Fortenberry JD, Kenney RD. Distal renal tubular acidosis as the initial manifestation of systemic lupus erythematosus in an adolescent. J Adolesc Health 1991;12:148–151.
[Article] [PubMed]4. Bagga A, Jain Y, Srivastava RN, Bhuyan UN. Renal tubular acidosis preceding systemic lupus erythematosus. Pediatr Nephrol 1993;7:735–736.
[Article] [PubMed]5. Ter Meulen CG, Pieters GF, Huysmans FT. Flaccid paresis due to distal renal tubular acidosis preceding systemic lupus erythematosus. Neth J Med 2002;60:29–32.
[PubMed]6. Koul PA, Wahid A, Shah BA. Systemic lupus erythematosus with distal renal tubular acidosis presenting as hypokalemic paralysis with respiratory failure. Saudi J Kidney Dis Transpl 2003;14:190–193.
[PubMed]7. Donckerwolcke RA. Diagnosis and treatment of renal tubular disorders in children. Pediatr Clin North Am 1982;29:895–906.
[PubMed]8. Caruana RJ, Buckalew VM Jr. The syndrome of distal (type 1) renal tubular acidosis. clinical and laboratory findings in 58 cases. Medicine (Baltimore) 1998;67:84–99.
[Article] [PubMed]9. Siamopoulos KC, Mavridis AK, Elisaf M, Drosos AA, Moutsopoulos HM. Kidney involvement in primary Sjögren's syndrome. Scand J Rheumatol Suppl 1986;61:156–160.10. Feest TG, Lockwood CM, Morley AR, Uff JS. Renal histology and immunopathology in distal renal tubular acidosis. Clin Nephrol 1978;10:187–190.
[PubMed]11. Gur H, Kopolovic Y, Gross DJ. Chronic predominant interstitial nephritis in a patient with systemic lupus erythematosus: a follow up of three years and review of the literature. Ann Rheum Dis 1987;46:617–623.
[Article] [PubMed] [PMC]12. Fang JT, Chen YC. Systemic lupus erythematosus presenting initially as hydrogen ATPase pump defects of distal renal tubular acidosis. Ren Fail 2000;22:647–652.
[Article] [PubMed]13. Tu WH, Shearn MA. Systemic lupus erythematosus and latent renal tubular dysfunction. Ann Intern Med 1967;67:100–109.
[Article] [PubMed]14. Graninger WB, Steinberg AD, Meron G, Smolen JS. Interstitial nephritis in patients with systemic lupus erythematosus: a manifestation of concomitant Sjögren's syndrome? Clin Exp Rheumatol 1991;9:41–45.
[PubMed]15. Ratner M, Wstenberg P, Serov VV, et al. Tubular function disturbances in chronic glomerulonephritis and their significance for identifying tubulointerstitial lesions. Nephron 1985;39:117–121.
[Article] [PubMed]16. Rahman A, Isenberg DA. Systemic lupus erythematosus. N Engl J Med 2008;358:929–939.
[Article] [PubMed]17. Cataudella JA, Young ID, Iliescu EA. Epstein-Barr virusassociated acute interstitial nephritis: infection or immunologic phenomenon? Nephron 2002;92:437–439.
[Article] [PubMed]18. Takemoto F, Katori H, Sawa N, et al. Induction of anti-carbonic -anhydrase-II antibody causes renal tubular acidosis in a mouse model of Sjögren's syndrome. Nephron Physiol 2007;106:63–68http://dx.doi.org/10.1159/000104873.
[Article] [PubMed]
